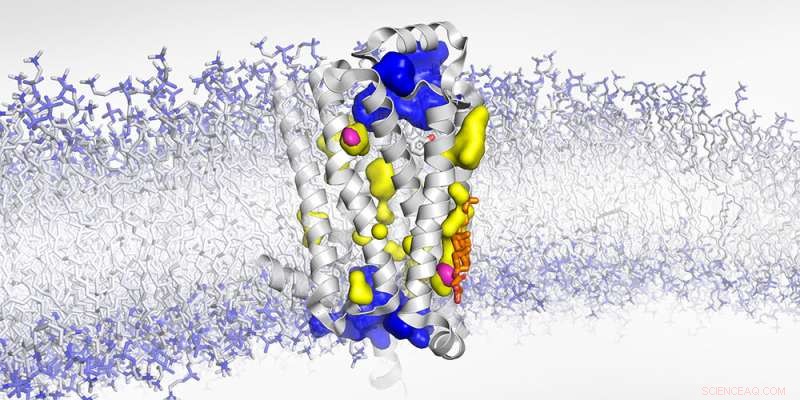
Struttura del recettore β1-adrenergico legato alla membrana con cavità esposte all'acqua (blu), non accessibili all'acqua (giallo) e vuoti secchi (magenta). Credito:Biozentrum, Università di Basilea
Quasi tutte le funzioni vitali del corpo umano sono regolate dai cosiddetti recettori accoppiati a proteine G sulla superficie cellulare. Questi recettori fungono quindi da interessanti bersagli farmacologici per il trattamento di varie malattie. I ricercatori hanno ora scoperto che gli spazi vuoti all'interno di questi recettori sono importanti per la loro attivazione e quindi per trasmettere messaggi alla cellula interna. Il loro approccio per individuare questi vuoti può aiutare a dirigere la ricerca di nuovi farmaci.
I recettori accoppiati alle proteine G (GPCR) ci consentono di vedere, assaggiare il cibo, sentire freddo o caldo o rispondere allo stress, tra le altre cose. Situati sulla superficie cellulare, i GPCR rilevano un'ampia varietà di segnali come nutrienti, luce, odori o ormoni. Modificando la loro conformazione, trasmettono queste informazioni dall'esterno all'interno della cellula. La conoscenza accumulata sui GPCR ha influenzato enormemente la medicina moderna:circa un terzo di tutti i farmaci commercializzati prende di mira i GPCR.
Spazi vuoti importanti per l'attivazione del recettore
Utilizzando una tecnologia all'avanguardia, il gruppo di ricerca guidato dal Prof. Stephan Grzesiek, insieme ai collaboratori del Biozentrum dell'Università di Basilea e dell'Istituto Paul Scherrer, ha ora scoperto che i GPCR contengono cavità completamente vuote che sono importanti per la loro attivazione. Il loro recente approccio sperimentale, pubblicato su Nature Chemistry , può indirizzare e accelerare la ricerca di nuovi e più specifici farmaci candidati con minori effetti collaterali.
Sebbene gli 826 GPCR all'interno del corpo umano rispondano a molti stimoli diversi, condividono tutti un'architettura comune. "Il nostro obiettivo è capire a livello atomico come i GPCR trasmettono segnali", afferma la dott.ssa Layara Abiko, che ha co-diretto lo studio. "Per molti anni, quindi, studiamo il recettore β1-adrenergico, un GPCR che prepara il corpo alla lotta o alla fuga". L'ormone adrenalina si lega e attiva il recettore che innesca una risposta allo stress, provocando ad esempio un aumento della frequenza cardiaca e della pressione sanguigna." I beta-bloccanti inibiscono questo recettore e quindi sono farmaci efficaci per il trattamento dell'ipertensione o delle malattie cardiovascolari.
Esatta localizzazione dei vuoti secchi
"Grazie all'NMR ad alta pressione e al nostro approccio sperimentale che utilizza la diffusione dei raggi X sui cristalli del recettore che incorporavano il gas nobile xeno, potremmo completare ulteriormente il quadro di questo recettore altamente dinamico", afferma Abiko. "In precedenza, si presumeva che le cavità all'interno del recettore fossero piene d'acqua. Ora abbiamo rivelato che alcune di esse sono vuote". Durante l'attivazione, la conformazione del recettore cambia in modo tale che questi vuoti secchi si comprimano e scompaiano. Di conseguenza, il recettore si restringe proprio come quando si schiaccia una spugna. Nel caso del recettore β1-adrenergico, questo cambiamento conformazionale è la chiave per avviare la risposta di lotta o fuga del corpo.
I ricercatori sono stati ora in grado di localizzare esattamente due di queste cavità vuote e hanno rivelato che il colesterolo, un importante componente della membrana cellulare, può riempire una di queste. Come un cuneo, il colesterolo impedisce al recettore di schiacciarsi e di passare al suo stato completamente attivo. "Bloccare questo vuoto ostruisce i movimenti sottili ma essenziali necessari per attivare il GPCR", spiega Abiko. "Pensiamo che questo effetto a cuneo potrebbe essere un altro livello di regolazione del recettore."
Nuove vie per lo sviluppo di farmaci
Ma perché lo scouting per i vuoti asciutti può essere importante? I siti di legame dei farmaci classici sono spesso simili tra le sottoclassi GPCR. Un farmaco diretto a tale sito può legarsi a più di un recettore e quindi causare effetti collaterali indesiderati. Al contrario, le cavità asciutte differiscono considerevolmente tra i GPCR, anche quando provengono dalla stessa sottoclasse. Questo li rende bersagli farmacologici altamente selettivi.
"In questo modo, puoi progettare farmaci altamente specifici per un recettore", spiega Abiko. Il nuovo approccio sviluppato può individuare tali siti di legame dei farmaci non convenzionali che differiscono fortemente tra i recettori. Questo può aiutare il processo di screening per nuove terapie, risparmiare tempo e ridurre i costi. + Esplora ulteriormente