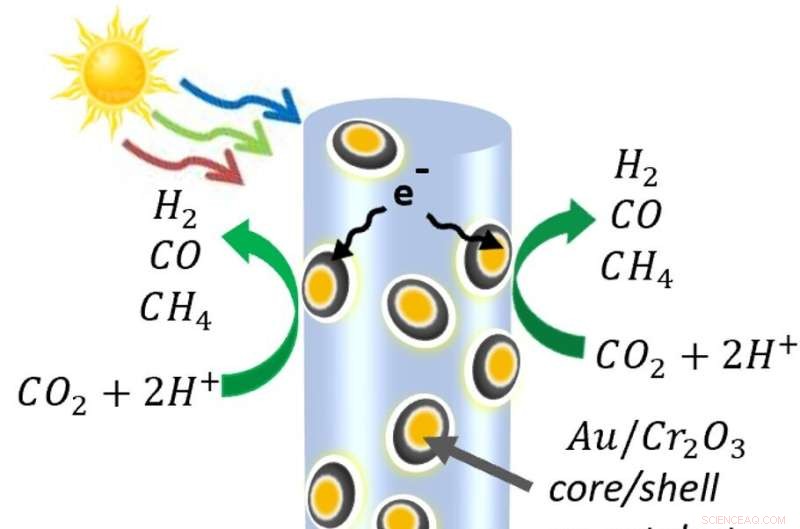
Un diagramma dei nanofili semiconduttori fatti di indio, gallio e azoto, decorati con nanoparticelle di oro e ossido di cromo. Quando la luce colpisce il nanofilo, libera gli elettroni e i "buchi" caricati positivamente che gli elettroni lasciano dietro di sé. Sul nanofilo stesso, i fori ossidano l'acqua in protoni (idrogeno) e ossigeno. Nel frattempo, alcuni elettroni vengono attirati nelle nanoparticelle metalliche, dove rompono l'anidride carbonica. Le molecole si ricombinano nelle molecole di monossido di carbonio, idrogeno e metano che compongono il syngas. Credito:Roksana Rashid, McGill University.
Il gas di sintesi a energia solare potrebbe riciclare l'anidride carbonica in combustibili e sostanze chimiche utili, ha dimostrato un team internazionale di ricercatori.
"Se siamo in grado di generare syngas dall'anidride carbonica utilizzando solo l'energia solare, possiamo utilizzarla come precursore del metanolo e di altre sostanze chimiche e combustibili. Ciò ridurrà significativamente la CO2 complessiva emissioni", ha affermato Zetian Mi, professore di ingegneria elettrica e informatica presso l'Università del Michigan, che ha condotto lo studio pubblicato negli Proceedings of the National Academy of Science .
Composto principalmente da idrogeno e monossido di carbonio con poco metano, il syngas è comunemente derivato da combustibili fossili con l'ausilio dell'elettricità. Inoltre, vengono spesso aggiunte sostanze chimiche tossiche per rendere il processo più efficiente.
"Il nostro nuovo processo è in realtà piuttosto semplice, ma è eccitante perché non è tossico, è sostenibile ed è molto conveniente", ha affermato Roksana Rashid, prima autrice dello studio, che ha eseguito gli esperimenti come studente di dottorato in ingegneria elettrica e informatica presso McGill University in Canada.
Per creare un processo che utilizza solo l'energia solare, il gruppo di Mi ha superato la difficoltà di scindere le molecole di anidride carbonica, che sono tra le più stabili dell'universo. Per questo, hanno arricchito una foresta di nanofili semiconduttori con nanoparticelle. Quelle nanoparticelle, fatte di oro rivestite di ossido di cromo, attiravano le molecole di anidride carbonica e le piegavano, indebolendo i legami tra carbonio e ossigeno.
I nanofili di nitruro di gallio hanno utilizzato l'energia luminosa per liberare gli elettroni e gli spazi caricati positivamente che lasciano dietro di sé, noti come buchi. I fori dividono le molecole d'acqua, separando i protoni (idrogeno) dall'ossigeno. Quindi, presso i catalizzatori metallici, gli elettroni dividono l'anidride carbonica, producendo monossido di carbonio e talvolta assorbendo l'idrogeno libero per produrre metano. Sono in fase di sviluppo processi per separare l'ossigeno dagli altri gas.
"La nostra tecnologia fa luce su come costruire una produzione distribuita di syngas da aria, acqua e luce solare", ha affermato Baowen Zhou, coautore dello studio con Mi ed ex ricercatore post-dottorato nel laboratorio di Mi presso la McGill University e l'UM.
Modificando il rapporto tra oro e ossido di cromo nelle nanoparticelle, il team di Mi è stato in grado di controllare le quantità relative di idrogeno e monossido di carbonio prodotte nella reazione. Questo è importante perché il rapporto tra idrogeno e monossido di carbonio influisce sulla facilità con cui è possibile produrre un tipo di carburante o sostanza chimica.
"Ciò che sorprende è la sinergia tra oro e ossido di cromo per creare la CO2 riduzione a syngas efficiente e sintonizzabile. Ciò non era possibile con un singolo catalizzatore metallico", ha affermato Mi. "Questo apre molte interessanti opportunità che non erano state considerate in precedenza".
La configurazione syngas sintonizzabile di Mi utilizza processi di produzione industriale standard ed è scalabile. Sebbene Rashid abbia utilizzato acqua distillata in questo esperimento, si prevede che anche l'acqua di mare e altre soluzioni elettrolitiche funzionino e Mi le ha utilizzate in studi correlati sulla divisione dell'acqua.
"Il semiconduttore che utilizziamo come assorbitore di luce è basato su silicio e nitruro di gallio, che sono i semiconduttori più comunemente prodotti, e utilizziamo pochissimo materiale per il nitruro di gallio. Ogni nanofilo ha uno spessore di circa un micrometro", ha affermato Mi.
Il prossimo obiettivo di Mi è aumentare l'efficienza del dispositivo, che attualmente si attesta allo 0,89%. Quando il 10% dell'energia luminosa viene convertito in energia chimica, spera che la tecnologia possa vedere la tecnologia adottata per l'energia rinnovabile, simile alle celle solari. + Esplora ulteriormente