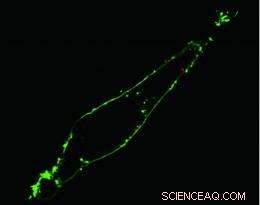
L'immagine confocale a fluorescenza di una singola cellula HeLa vivente mostra che tramite la nanoendoscopia un cluster di punti quantici (punto rosso) è stato consegnato al citoplasma all'interno della membrana (verde) della cellula. Per gentile concessione di Berkeley Lab
(PhysOrg.com) -- Un endoscopio in grado di fornire immagini ottiche ad alta risoluzione dell'interno di una singola cellula vivente, o consegnare con precisione i geni, proteine, farmaci terapeutici o altro carico senza ferire o danneggiare la cellula, è stato sviluppato da ricercatori con il Lawrence Berkeley National Laboratory (Berkeley Lab). Questa sonda ottica basata su nanofili altamente versatile e meccanicamente robusta può essere applicata anche al biosensore e all'elettrofisiologia a cella singola.
Un team di ricercatori del Berkeley Lab e dell'Università della California (UC) Berkeley ha collegato una guida d'onda di nanofili di ossido di stagno all'estremità rastremata di una fibra ottica per creare un nuovo sistema di endoscopi. La luce che viaggia lungo la fibra ottica può essere efficacemente accoppiata al nanofilo dove viene riemessa nello spazio libero quando raggiunge la punta. La punta del nanofilo è estremamente flessibile grazie alle sue dimensioni ridotte e all'elevato rapporto di aspetto, tuttavia può sopportare ripetute piegature e deformazioni in modo che possa essere utilizzato più volte.
"Combinando i vantaggi delle guide d'onda a nanofili e dell'imaging a fluorescenza in fibra ottica, possiamo manipolare la luce su scala nanometrica all'interno delle cellule viventi per studiare i processi biologici all'interno di singole cellule viventi con un'elevata risoluzione spaziale e temporale, "dice Peidong Yang, un chimico con la divisione di scienze dei materiali del Berkeley Lab, che ha condotto questa ricerca. "Abbiamo dimostrato che il nostro endoscopio basato su nanofili può anche rilevare segnali ottici da regioni subcellulari e, attraverso meccanismi attivati dalla luce, può fornire carichi utili in celle con specificità spaziale e temporale."
Yang, che ricopre anche incarichi con il Dipartimento di Chimica dell'Università della California Berkeley e il Dipartimento di Scienza e Ingegneria dei Materiali, è l'autore corrispondente di un articolo sulla rivista Nanotecnologia della natura descrivendo questo lavoro intitolato "Endoscopia unicellulare basata su nanowire". I co-autori del documento erano Ruoxue Yan, Parco Ji-Ho, Yeonho Choi, Chul-Joon Heo, Seung-Man Yang e Luke Lee.
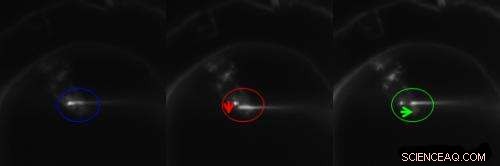
Immagini di un endoscopio a nanofili a stretto contatto con un cluster di punti quantici in una cella HeLa (a sinistra), e separati verticalmente dal cluster di 2 mm (al centro) e orizzontalmente da 6 mm (a destra). Cerchi e frecce colorate indicano la posizione del cluster e il movimento dell'endoscopio.
Nonostante i significativi progressi nella microscopia elettronica e a scansione di sonda, la microscopia a luce visibile rimane il cavallo di battaglia per lo studio delle cellule biologiche. Poiché le celle sono otticamente trasparenti, possono essere ripresi in modo non invasivo con luce visibile in tre dimensioni. Anche, la luce visibile consente l'etichettatura fluorescente e il rilevamento dei costituenti cellulari, come proteine, acidi nucleici e lipidi. L'unico inconveniente dell'imaging a luce visibile in biologia è stata la barriera di diffrazione, che impedisce alla luce visibile di risolvere strutture inferiori alla metà della lunghezza d'onda della luce incidente. Le recenti scoperte nella nanofotonica hanno permesso di superare questa barriera e di rendere visibili i componenti subcellulari con i sistemi di imaging ottico. Però, tali sistemi sono complessi, costoso e, abbastanza stranamente, di dimensioni ingombranti.
"In precedenza, abbiamo dimostrato che le guide d'onda a nanofili dielettrici a lunghezza d'onda inferiore possono trasportare efficacemente la luce ultravioletta e visibile nell'aria e nei mezzi fluidi, " Yang dice. "Incorporando uno dei nostri componenti nanofotonici in un semplice, basso costo, installazione in fibra ottica da banco, siamo stati in grado di miniaturizzare il nostro sistema endoscopico."
Per testare il loro endoscopio a nanofili come fonte di luce locale per l'imaging subcellulare, Yang e i suoi coautori l'hanno accoppiato otticamente a un laser di eccitazione, quindi hanno condotto la luce blu a guida d'onda attraverso la membrana e all'interno delle singole cellule HeLa, la linea cellulare umana immortalizzata più comunemente usata per la ricerca scientifica.
"L'uscita ottica dall'emissione dell'endoscopio era strettamente confinata alla punta del nanofilo e quindi offriva un'illuminazione altamente direzionale e localizzata, " Yang dice. "L'inserimento del nostro nanofilo di ossido di stagno nel citoplasma cellulare
non ha indotto la morte cellulare, apoptosi, stress cellulare significativo, o rottura della membrana. Inoltre, illuminare l'ambiente intracellulare delle cellule HeLa con luce blu usando la nanosonda non ha danneggiato le cellule perché il volume di illuminazione era così piccolo, fino alla scala del picolitro."
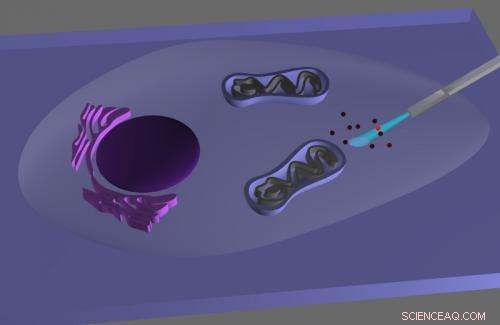
Questo schema illustra l'imaging subcellulare di punti quantici in una cellula vivente utilizzando un endoscopio a nanofili. Credito:(per gentile concessione di Berkeley Lab)
Dopo aver dimostrato la biocompatibilità del loro endoscopio a nanofili, Yang e i suoi coautori hanno poi testato le sue capacità di consegnare carichi utili a siti specifici all'interno di una cella. Mentre sono stati segnalati sistemi di consegna a cella singola basati su nanotubi di nitruro di carbonio e boro, questi sistemi soffrono di tempi di consegna che vanno dai 20 ai 30 minuti, più una mancanza di controllo temporale sul processo di consegna. Per superare questi limiti, Yang e i suoi coautori hanno attaccato punti quantici alla punta del nanofilo di ossido di stagno del loro endoscopio utilizzando linker fotoattivati che possono essere tagliati da radiazioni ultraviolette a bassa potenza. Entro un minuto, il loro endoscopio a nanofili funzionalizzato è stato in grado di rilasciare il suo carico di punti quantici nei siti intracellulari mirati.
"La scansione al microscopio confocale della cellula ha confermato che i punti quantici sono stati consegnati con successo oltre la membrana etichettata in modo fluorescente e nel citoplasma, " Yang dice. "La fotoattivazione per rilasciare i punti non ha avuto effetti significativi sulla vitalità cellulare".
La luce laser blu altamente direzionale è stata utilizzata per eccitare uno dei due cluster di punti quantici che si trovavano a soli due micrometri di distanza. Con l'area di illuminazione stretta e la piccola separazione tra la sorgente luminosa e i punti, sono state garantite una bassa fluorescenza di fondo e un elevato contrasto delle immagini.
"Nel futuro, oltre all'imaging ottico e alla consegna del carico, potremmo anche usare questo endoscopio a nanofili per stimolare elettricamente o otticamente una cellula vivente, " dice Yang.
I nanofili utilizzati in questi esperimenti sono stati originariamente sviluppati per studiare nuove proprietà elettroniche e ottiche dipendenti dalle dimensioni per applicazioni energetiche.