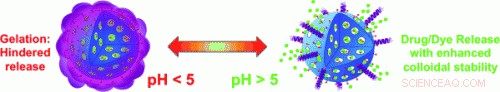
(Phys.org)—Come possono i prodotti farmaceutici essere trasportati in sicurezza attraverso l'ambiente acido dello stomaco e nell'intestino? Un team di ricercatori canadesi e australiani ha sviluppato un nuovo nanotrasportatore costituito da particelle porose di biossido di silicio stabilizzate con una proteina del siero di latte. In ambienti acidi la proteina forma un gel che chiude i pori; a valori di pH più elevati, i pori sono aperti.
Per i prodotti farmaceutici, sia il farmaco stesso che la sua forma di somministrazione sono importanti, poiché quest'ultimo determina dove e quando il farmaco diventa attivo nel corpo. Per esempio, le formulazioni a rilascio prolungato sono progettate per mantenere un livello costante del farmaco per un periodo di tempo più lungo e i farmaci antitumorali sono pensati per diventare attivi nelle cellule malate nel modo più selettivo possibile al fine di ridurre al minimo gli effetti collaterali. Per far funzionare questo i farmaci devono essere "confezionati" correttamente. Il confezionamento è spesso richiesto anche per i farmaci somministrati per via orale perché molti farmaci vengono distrutti dall'acido dello stomaco prima che possano raggiungere l'intestino per essere assorbiti nel flusso sanguigno. Però, la protezione contro l'acido deve anche rilasciare il farmaco nelle condizioni riscontrate nell'intestino.
Un tipo molto promettente di "pacchetto" di farmaci è la nanoparticella di biossido di silicio mesoporoso. Questi sono biocompatibili e facili da realizzare con le dimensioni dei pori e delle particelle richieste. La chimica delle loro superfici interne ed esterne può essere facilmente modificata, possono essere facilmente caricati con molecole di farmaco di varie dimensioni, e questi possono a loro volta essere rilasciati in modo controllato. Però, queste particelle hanno la tendenza ad aggregarsi in condizioni fisiologiche, che possono cambiare completamente le loro proprietà. Anche, devono essere sviluppati nuovi metodi per garantire il rilascio selettivo al target desiderato. Il cambiamento di pH nella transizione dallo stomaco all'intestino è un potenziale fattore scatenante.
Un team guidato da Shi Zhang Qiao presso l'Università del Queensland (Brisbane, Australia) e Freddy Kleitz all'Université Laval (Quebec, Canada) ha ora raffinato alcuni nanotrasportatori di biossido di silicio, riportano nella rivista Angewandte Chemie. Il loro successo deriva dal loro uso di -lattoglobulina, una proteina del siero utilizzata come integratore alimentare. I ricercatori hanno attaccato questo alla superficie esterna delle nanoparticelle porose, impedendone l'aggregazione e aumentandone la biocompatibilità. A valori di pH inferiori a 5, come quelli che si trovano nello stomaco, Gel di β-lattoglobulina:si gonfia e forma un "guscio" di gelatina attorno alle nanoparticelle, che ostruisce i pori e impedisce al farmaco di uscire. A valori di pH più elevati come quelli dell'intestino, la proteina assume la forma di molecole discrete, aprendo i pori e rilasciando il farmaco.
Oltre allo stomaco e all'intestino, anche altri organi hanno valori di pH diversi e ci sono persino differenze di pH tra alcuni tumori e il tessuto sano circostante. L'ulteriore sviluppo di questa nuova procedura potrebbe essere utilizzato per realizzare nanotrasportatori in grado di reagire a tali gradienti di pH più sottili.