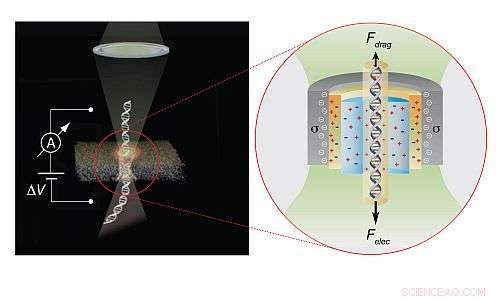
L'effetto optoelettrico può essere utilizzato per controllare il passaggio di molecole di DNA attraverso sensori a nanopori, portando così a un rilevamento e un sequenziamento più accurati delle singole molecole di DNA.
Un giorno, i medici saranno in grado di creare piani di trattamento medico personalizzati basati sul DNA di un paziente, individuare la radice della malattia di un paziente e assicurarsi che il trattamento non causi una reazione allergica fatale. Grazie al professor Amit Meller del Technion, la fantasia è un passo più vicino alla realtà
La chiave per realizzare questa medicina rivoluzionaria basata sul DNA è la decodifica rapida e accurata del genoma di un paziente. Un genoma è la sequenza unica di molecole speciali lungo una catena di DNA che dice al macchinario di una cellula quali proteine produrre, e quando. Quelle molecole cruciali del genoma sono chiamate "nucleobasi, " e sono conosciuti come adenina, timina, citosina, e guanina (o A, T, C, e G, in breve). Il prof. Meller e il suo team hanno sviluppato un modo per registrare l'As, Ts, Cs, e Gs nel DNA di una persona costringendo una molecola di DNA a scivolare attraverso un minuscolo foro - chiamato "nanoporo" - in un minuscolo chip di silicio delle dimensioni della testa di un chiodo.
(Quanto è piccolo un nanoporo? Misura tra 2 e 5 nanometri, o miliardesimi di metro, di diametro. In confronto, un capello umano misura 100 micrometri, o milionesimi di metro, di diametro.)
Gli scienziati iniziano immergendo le molecole di DNA in una combinazione di acqua e molecole di sale caricate elettricamente. Mentre l'acqua salata scorre attraverso il nanoporo, crea una corrente elettrica. Quando una molecola di DNA passa attraverso il poro, però, la corrente è interrotta. E, la quantità di interruzione di corrente dipende da quale A, T, C, o G è nel poro.
Perciò, leggere la sequenza delle basi azotate, uno scienziato deve semplicemente scoprire quanto ogni base interrompe la corrente elettrica. Con quelle informazioni, poteva leggere la sequenza delle basi del DNA semplicemente registrando la sequenza delle interruzioni elettriche al passaggio di una molecola di DNA. c'è un problema, anche se. "Per fare questo, ogni base deve rimanere nel poro abbastanza a lungo da rendere molto chiaro quanta corrente blocca, in modo che si possa identificare correttamente la base azotata, "dice il prof. Meller.
Ma il DNA di solito si muove troppo velocemente attraverso i nanopori perché Meller e il suo team possano decodificarlo. Per rallentare il DNA, brillavano un laser verde - non più forte dei puntatori laser usati nelle aule - al poro, che gli dava una carica elettrica negativa. Il nanoporo ha quindi attratto gli atomi di potassio caricati positivamente nell'acqua salata. Quegli atomi, insieme a un po' d'acqua, spostato verso il poro, creando un flusso che bloccava il movimento del DNA. "Così, che crea una forza di trascinamento sul DNA, rallentandolo in modo che ogni base rimanga più a lungo nel nanoporo, " dice il prof. Meller.
Questo metodo di lettura delle sequenze di DNA è ancora in fase di sviluppo in laboratorio. Ma Meller immagina un futuro in cui il chip nanoporo potrebbe essere integrato in un dispositivo portatile, delle dimensioni di uno smartphone, che potrebbe essere portato direttamente al paziente.
Il team di ricerca Technion ha collaborato con i colleghi della Boston University su questo progetto. I risultati del team sono stati pubblicati nell'edizione online del 3 novembre di Nanotecnologia della natura .