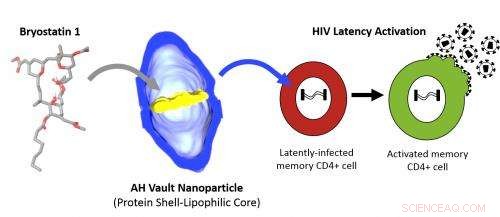
Gli scienziati dell'UCLA hanno sviluppato un metodo per posizionare la briostatina 1 in depositi su scala nanometrica per una consegna sicura alle cellule, dove può attivare l'HIV latente, permettendo al virus di essere debellato.
(Phys.org) —Un team multidisciplinare di scienziati dell'UCLA e della Stanford University ha utilizzato una nanoparticella naturale chiamata vault per creare un nuovo sistema di somministrazione di farmaci che potrebbe portare a progressi nel trattamento del cancro e dell'HIV.
Il gruppo di ricerca è stato guidato dal Dr. Leonard Rome, direttore associato del California NanoSystems Institute dell'UCLA, e il dottor Jerome Zack, co-direttore dell'UCLA AIDS Institute, entrambi sono anche membri del Jonsson Comprehensive Cancer Center dell'UCLA. Co-primi autori dello studio sono stati Daniel Buehler, un ricercatore post-dottorato dell'UCLA e Matthew Marsden, professore assistente aggiunto nel dipartimento di medicina e membro dell'AIDS Institute.
Le loro scoperte potrebbero portare a trattamenti contro il cancro più efficaci con dosi più piccole ea terapie che potrebbero potenzialmente sradicare il virus dell'HIV.
Il documento è la storia di copertina dell'edizione cartacea del 26 agosto della rivista ACSNano, ed è stato recentemente pubblicato online.
Rome e la sua allora studentessa post-dottorato Nancy Kedersha hanno scoperto i caveau negli anni '80. Le nanoparticelle naturali sono migliaia all'interno di ciascuna delle nostre cellule. Una nanoparticella è una sostanza minuscola, in questo caso costituito da proteine, che si misura in nanometri (1 nanometro equivale a 1 miliardesimo di metro).
Negli anni, Rome e i suoi collaboratori hanno scoperto come creare volte in laboratorio utilizzando le proteine di cui sono costituiti. Le volte naturali contenevano altri elementi, ma la Roma ne ha costruite di vuote, che alla fine ha permesso loro di perseguire l'idea di inserire molecole di farmaco all'interno in modo che potessero essere iniettate in un paziente e indirizzate a cellule specifiche, dove avrebbero rilasciato i farmaci.
Il prossimo obiettivo di Roma era quello di migliorare i farmaci chemioterapici esistenti, che uccidono le cellule cancerose, ma causano anche effetti collaterali perché sono tossici anche per i tessuti sani. Rome e il suo team hanno teorizzato che l'uso di caveau per somministrare farmaci direttamente alle cellule tumorali eliminerebbe il contatto dei farmaci con le cellule sane e dovrebbe ridurre notevolmente gli effetti collaterali del trattamento. Questo concetto deve ancora essere dimostrato negli esseri umani, ma i ricercatori sono ora più vicini agli studi clinici sulla tecnologia di consegna del caveau.
Un altro obiettivo era l'HIV/AIDS, che negli ultimi anni è passata dall'essere una condanna a morte a una malattia cronica man mano che i cocktail di farmaci antiretrovirali sono migliorati. Però, per le persone con HIV/AIDS, il mantenimento della salute richiede ancora che prendano i farmaci per tutta la vita, a causa di un fenomeno chiamato latenza dei provirus all'interno dei serbatoi cellulari.
Ciò significa che nonostante la carica virale, o livello del sangue, dell'HIV ridotto a livelli non rilevabili dai farmaci, il virus latente (inattivo) si accumula ancora all'interno delle cellule in tasche chiamate serbatoi cellulari. Poiché i farmaci per l'HIV possono colpire solo i virus attivi, questi serbatoi di virus latenti sopravvivono al trattamento farmacologico. Quando i farmaci antiretrovirali vengono sospesi, il virus latente si attiva, aumentando la carica virale e sostanzialmente riaccendendo l'infezione da HIV.
La sfida per Zack e Marsden era come affrontare quei serbatoi latenti di cellule HIV, che impediscono l'eradicazione dell'HIV nei pazienti trattati. I ricercatori hanno scoperto che un modo per eliminare i serbatoi era attivare l'HIV latente, rendendolo suscettibile ai farmaci antivirali. Sapevano che un farmaco chiamato briostatina 1 attivava l'HIV latente in laboratorio, ma l'idea di darlo ai pazienti era problematica a causa dei suoi effetti collaterali tossici.
Zack e Marsden avevano bisogno di un modo per somministrare il farmaco riducendo al minimo gli effetti collaterali, rendendolo un candidato perfetto per la consegna nel caveau.
Roma e Buehler hanno bioingegnerizzato una volta con uno speciale nucleo lipofilo, che lega i lipidi e quindi crea un ambiente che consente il caricamento di composti come la briostatina 1 nelle volte. Con Zack, Marsden e Paul Wender della Stanford University, hanno dimostrato che il caveau poteva contenere la briostatina 1 e rilasciarla quando consegnata alle cellule contenenti i serbatoi di HIV latenti. Il team sta portando avanti ulteriori studi per avvicinare ai test clinici gli attivatori del virus latente caricati nel caveau.
"Poiché il virus latente non è curabile, i serbatoi latenti sono il principale ostacolo alla cura dell'HIV in questo momento, " ha detto Zack, che è anche professore di medicina e microbiologia, immunologia e genetica molecolare. "Se riusciamo ad attivare il virus latente, essenzialmente accendendolo, possiamo curarlo e sradicarlo, curando così il paziente dall'infezione da HIV".
"Questi esperimenti dimostrano la nuova capacità di queste volte di incapsulare composti terapeutici fino a più di 2, 000 molecole per singolo caveau, " disse Roma, anche un professore UCLA di biochimica. "E questi particolari caveau possono interiorizzare completamente il loro carico, aggiungendo un ulteriore livello di protezione per le cellule sane".