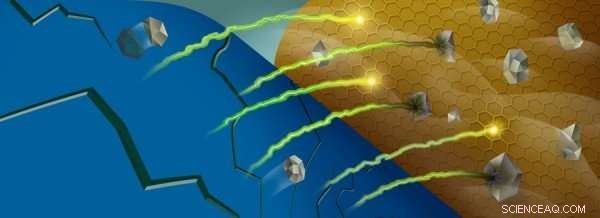
Quando gli ioni manganese (grigio) vengono rimossi dal catodo di una batteria (blu), possono reagire con l'elettrolita della batteria vicino all'anodo (oro), intrappolare gli ioni di litio (verde/giallo). Credito:Robert Horn/Laboratorio nazionale Argonne
Come te, io e tutti quelli che conosciamo, le batterie hanno una durata limitata.
Quando una batteria entra nella "vecchiaia, " gli scienziati si riferiscono alla sua riduzione delle prestazioni come "capacità dissolvenza, " in cui la quantità di carica che una batteria può fornire diminuisce con l'uso ripetuto. La diminuzione della capacità è il motivo per cui una batteria del telefono cellulare che durava un'intera giornata, dopo un paio d'anni, durano forse solo poche ore.
Ma cosa accadrebbe se gli scienziati potessero ridurre questa capacità svanire, permettendo alle batterie di invecchiare con più grazia?
"Ora che conosciamo i meccanismi alla base dell'intrappolamento degli ioni di litio e la diminuzione della capacità, possiamo trovare metodi per risolvere il problema."
I ricercatori dell'Argonne National Laboratory del Dipartimento dell'Energia degli Stati Uniti (DOE) hanno identificato uno dei principali colpevoli della diminuzione della capacità delle batterie agli ioni di litio ad alta energia in un articolo pubblicato su The Journal of the Electrochemical Society.
Per una batteria agli ioni di litio, del tipo che usiamo nei laptop, smartphone, e veicoli elettrici ibridi plug-in:la capacità della batteria è direttamente legata alla quantità di ioni di litio che possono essere trasportati avanti e indietro tra i due terminali della batteria mentre viene caricata e scaricata.
Questa spola è consentita da alcuni ioni di metalli di transizione, che cambiano gli stati di ossidazione quando gli ioni di litio entrano ed escono dal catodo. Però, mentre la batteria viene ricaricata, alcuni di questi ioni, in particolare il manganese, vengono rimossi dal materiale del catodo e finiscono nell'anodo della batteria.
Una volta vicino all'anodo, questi ioni metallici interagiscono con una regione della batteria chiamata interfase solido-elettrolita, che si forma a causa delle reazioni tra l'anodo altamente reattivo e l'elettrolita liquido che trasporta avanti e indietro gli ioni di litio. Per ogni molecola di elettrolita che reagisce e si decompone in un processo chiamato riduzione, uno ione di litio rimane intrappolato nell'interfase. Man mano che sempre più litio viene intrappolato, la capacità della batteria diminuisce.
Alcune molecole in questa interfase sono ridotte in modo incompleto, il che significa che possono accettare più elettroni e legare ancora più ioni di litio. Queste molecole sono come esca, in attesa di una scintilla.
Quando gli ioni manganese si depositano in questa interfase agiscono come una scintilla che accende l'esca:questi ioni sono efficienti nel catalizzare le reazioni con le molecole non completamente ridotte, intrappolando più ioni di litio nel processo.
"C'è una stretta correlazione tra la quantità di manganese che arriva all'anodo e la quantità di litio che rimane intrappolata, " ha detto il coautore dello studio e scienziato di Argonne Daniel Abraham. "Ora che conosciamo i meccanismi alla base dell'intrappolamento degli ioni di litio e la capacità svanisce, possiamo trovare metodi per risolvere il problema."