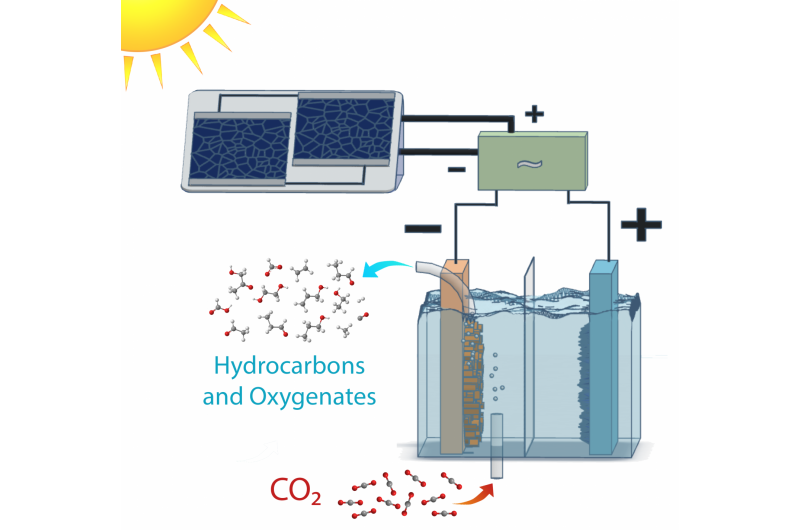
Schema di una cella di elettrolisi a energia solare che converte l'anidride carbonica in prodotti idrocarburici e ossigenati con un'efficienza di gran lunga superiore alla fotosintesi naturale. L'elettronica di adattamento della potenza consente al sistema di funzionare in una gamma di condizioni solari. Credito:Clarissa Towle/Berkeley Lab
Gli scienziati del Lawrence Berkeley National Laboratory (Berkeley Lab) del Dipartimento dell'Energia hanno sfruttato il potere della fotosintesi per convertire l'anidride carbonica in combustibili e alcoli con efficienze di gran lunga superiori a quelle delle piante. Il risultato segna una pietra miliare significativa nello sforzo di passare a fonti di carburante sostenibili.
Molti sistemi hanno ridotto con successo l'anidride carbonica a precursori chimici e di carburante, come il monossido di carbonio o una miscela di monossido di carbonio e idrogeno noto come syngas. Questo nuovo lavoro, descritto in uno studio pubblicato sulla rivista Scienze energetiche e ambientali , è il primo a dimostrare con successo l'approccio di passare dall'anidride carbonica direttamente ai prodotti mirati, vale a dire etanolo ed etilene, a efficienze di conversione energetica che rivaleggiano con le controparti naturali.
I ricercatori hanno fatto questo ottimizzando ogni componente di un sistema elettrochimico fotovoltaico per ridurre la perdita di tensione, e creare nuovi materiali quando quelli esistenti non bastavano.
"Questo è uno sviluppo entusiasmante, " ha detto il ricercatore principale dello studio Joel Ager, uno scienziato del Berkeley Lab con incarichi congiunti nelle divisioni Scienze dei materiali e Scienze chimiche. "Poiché l'aumento dei livelli di CO2 atmosferica cambia il clima della Terra, la necessità di sviluppare fonti di energia sostenibili è diventata sempre più urgente. Il nostro lavoro qui mostra che abbiamo un percorso plausibile per produrre combustibili direttamente dalla luce solare".
Quel percorso dal sole al carburante è tra gli obiettivi chiave del Centro comune per la fotosintesi artificiale (JCAP), un DOE Energy Innovation Hub istituito nel 2010 per far progredire la ricerca sui combustibili solari. Lo studio è stato condotto presso il campus Berkeley Lab di JCAP.
L'obiettivo iniziale della ricerca JCAP era affrontare l'efficiente scissione dell'acqua nel processo di fotosintesi. Avendo ampiamente raggiunto tale compito utilizzando diversi tipi di dispositivi, Gli scienziati JCAP che effettuano la riduzione dell'anidride carbonica azionata dal sole hanno iniziato a puntare al raggiungimento di efficienze simili a quelle dimostrate per la scissione dell'acqua, considerata da molti come la prossima grande sfida nella fotosintesi artificiale.
Un altro gruppo di ricerca del Berkeley Lab sta affrontando questa sfida concentrandosi su un componente specifico in un sistema fotovoltaico-elettrochimico. In uno studio pubblicato oggi, descrivono un nuovo catalizzatore in grado di ottenere la conversione dell'anidride carbonica in multicarbonio utilizzando input di energia record.
Non solo per mezzogiorno
Per questo studio JCAP, i ricercatori hanno progettato un sistema completo per lavorare in diversi momenti della giornata, non solo a un livello di energia luminosa pari all'illuminazione di 1 sole, che equivale al picco di luminosità a mezzogiorno in una giornata di sole. Hanno variato la luminosità della sorgente luminosa per mostrare che il sistema è rimasto efficiente anche in condizioni di scarsa illuminazione.
Quando i ricercatori hanno accoppiato gli elettrodi a celle fotovoltaiche in silicio, hanno raggiunto efficienze di conversione solare dal 3 al 4% per un'illuminazione da 0,35 a 1 sole. Modificando la configurazione in una ad alte prestazioni, La cella solare tandem collegata in tandem ha prodotto un'efficienza di conversione in idrocarburi e ossigenati superiore al 5% con illuminazione di 1 sole.

A sinistra è una vista superficiale di un catodo bimetallico di nanocorallo rame-argento preso da una micrografia elettronica a scansione. A destra c'è un'immagine a raggi X a dispersione di energia del catodo con il rame (in rosa/rosso) e l'argento (in verde) evidenziati. Credito:Gurudayal/Berkeley Lab
"Abbiamo fatto un piccolo ballo in laboratorio quando abbiamo raggiunto il 5 percento, " disse Ager, che detiene anche un incarico come professore a contratto presso il dipartimento di scienza e ingegneria dei materiali della UC Berkeley.
Tra i nuovi componenti sviluppati dai ricercatori c'è un catodo di nanocorallo rame-argento, che riduce l'anidride carbonica ad idrocarburi e ossigenati, e un anodo di nanotubi di ossido di iridio, che ossida l'acqua e crea ossigeno.
"La bella caratteristica del nanocorallo è che, come piante, può rendere i prodotti target in un'ampia gamma di condizioni, ed è molto stabile, " disse Ager.
I ricercatori hanno caratterizzato i materiali presso il National Center for Electron Microscopy presso la Molecular Foundry, un DOE Office of Science User Facility presso il Berkeley Lab. I risultati li hanno aiutati a capire come funzionavano i metalli nel catodo bimetallico. Nello specifico, hanno appreso che l'argento aiuta nella riduzione dell'anidride carbonica in monossido di carbonio, mentre il rame si riprende da lì per ridurre ulteriormente il monossido di carbonio a idrocarburi e alcoli.
cercando di meglio, rotture a bassa energia
Poiché l'anidride carbonica è una molecola ostinatamente stabile, romperlo in genere comporta un significativo apporto di energia.
"La riduzione della CO2 a un prodotto finale idrocarburico come l'etanolo o l'etilene può richiedere fino a 5 volt, dall'inizio alla fine, ", ha affermato l'autore principale dello studio Gurudayal, borsista post-dottorato al Berkeley Lab. "Il nostro sistema lo ha ridotto della metà mantenendo la selettività dei prodotti".
In particolare, gli elettrodi hanno funzionato bene in acqua, un ambiente a pH neutro.
"I gruppi di ricerca che lavorano sugli anodi lo fanno principalmente utilizzando condizioni alcaline poiché gli anodi richiedono in genere un ambiente a pH elevato, che non è l'ideale per la solubilità della CO2, " ha detto Gurudayal. "È molto difficile trovare un anodo che funzioni in condizioni neutre."
I ricercatori hanno personalizzato l'anodo facendo crescere i nanotubi di ossido di iridio su una superficie di ossido di zinco per creare una superficie più uniforme per supportare meglio le reazioni chimiche.
"Elaborando ogni passaggio con tanta attenzione, questi ricercatori hanno dimostrato un livello di prestazioni ed efficienza che le persone non pensavano fosse possibile a questo punto, ", ha affermato Frances Houle, chimica del Berkeley Lab, Vicedirettore JCAP per l'integrazione della scienza e della ricerca, che non faceva parte dello studio. "Questo è un grande passo avanti nella progettazione di dispositivi per la riduzione efficiente della CO2 e la sperimentazione di nuovi materiali, e fornisce un quadro chiaro per il futuro avanzamento di dispositivi di riduzione della CO2 completamente integrati a energia solare."