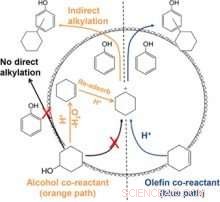
L'alchilazione del fenolo con il cicloesanolo (percorso arancione) avviene dopo che la maggior parte del cicloesanolo è disidratata a cicloesene. Il motivo per cui il meccanismo segue questo percorso non è dovuto all'accesso limitato al cicloesanolo, piuttosto è dovuto alla mancanza di un elettrofilo reattivo quando è presente una grande frazione di cicloesanolo. Credito:American Chemical Society
Benzina, lubrificanti, e i prodotti di consumo sono migliorati dagli additivi chimici. La produzione di additivi spesso comporta una reazione chimica nota come alchilazione, l'aggiunta di una catena di carbonio alle molecole esistenti. I chimici sanno che i catalizzatori acidi sono utili per l'alchilazione, ma come uno dei catalizzatori più popolari, zeoliti acide, eseguire l'alchilazione in una fase condensata non è ben compreso.
Jian Zhi Hu, Zhenchao Zhao, Hui Shi, Johannes Lercher, ei loro colleghi del Pacific Northwest National Laboratory hanno identificato un meccanismo di reazione chiave associato all'alchilazione del fenolo catalizzata da zeolite con cicloesanolo. Hanno fatto questa scoperta usando la spettroscopia di risonanza magnetica nucleare (MAS-NMR) in situ ad alta temperatura e alta pressione.
Gli scienziati ora hanno una comprensione di come l'attività catalitica, meccanismo, e le vie di reazione dipendono da tre fattori. Questi fattori sono la concentrazione e la forza dei siti acidi, i vincoli sterici per la reazione, e l'identità dell'agente alchilante.
Analisi cinetiche e spettroscopiche dettagliate hanno mostrato che l'alchilazione del fenolo con cicloesanolo non si verifica in modo apprezzabile prima che la maggior parte del cicloesanolo sia stata disidratata in cicloesene. Le reazioni di alchilazione sono rallentate finché è presente l'alcol. In contrasto, i prodotti di alchilazione si formano facilmente quando la soluzione contiene inizialmente solo fenolo e cicloesene.
Una combinazione di spettroscopia MAS-NMR in situ e l'uso di fenolo e cicloesanolo arricchiti con isotopi di carbonio-13 hanno permesso di identificare il percorso di reazione che è difficile da sondare con altri metodi di spettroscopia. La sequenza di reazione non si verifica come risultato dell'adsorbimento competitivo ma per l'assenza di un elettrofilo reattivo. Ciò è dovuto alla formazione preferenziale di complessi di adsorbimento, cioè., dimeri di alcol protonato nei siti dell'acido di Brønsted, che ostacolano l'assorbimento del cicloesene. A bassa copertura dei siti acidi da parte di dimeri protonati, l'adsorbimento e la protonazione del cicloesene produce ioni cicloesil carbenio, che attaccano il fenolo per produrre prodotti alchilati. Ciò implica inoltre che i dimeri di cicloesanolo protonato si disidratano senza la formazione di ioni carbenio.
I risultati mostrano l'importanza della spettroscopia NMR come metodo analitico in situ unico, fornendo informazioni molecolari dettagliate sul campione studiato in condizioni reali (operando).
"Esperti in catalisi e NMR hanno lavorato insieme per permetterci di osservare importanti processi chimici che si verificano ad alte temperature e pressioni, " ha detto Karl Mueller, Direttore scientifico e tecnologico del PNNL per le scienze fisiche e computazionali. "Prima, dovevamo dedurre cosa stava succedendo arrestando la reazione (cioè, ex situ) o solo misurando i prodotti finali, nessuno dei quali può mostrarci un quadro completo."
Con approfondimenti sui percorsi di reazione cruciali e su come la spettroscopia NMR può contribuire, il team sta continuando a esplorare nuove reazioni e catalizzatori per produrre vettori energetici, o molecole che immagazzinano energia nei legami chimici.