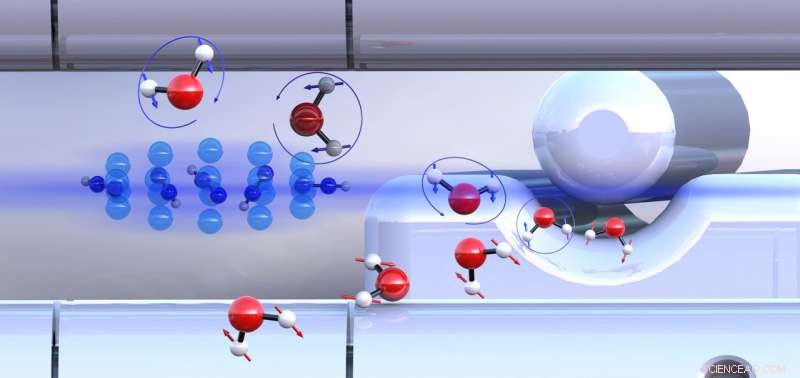
Le molecole orto-acqua e para-acqua preordinate con spin nucleari diversamente orientati (frecce blu o rosse) reagiscono con gli ioni diazenilio (centro sinistra) a velocità diverse. Credito:Università di Basilea
Le molecole d'acqua esistono in due forme diverse con proprietà fisiche quasi identiche. Per la prima volta, i ricercatori sono riusciti a separare le due forme per dimostrare che possono esibire diverse reattività chimiche. Questi risultati sono stati riportati dai ricercatori dell'Università di Basilea e dai loro colleghi ad Amburgo sulla rivista scientifica Comunicazioni sulla natura .
Dal punto di vista chimico, l'acqua è una molecola in cui un singolo atomo di ossigeno è legato a due atomi di idrogeno. È meno noto che l'acqua esiste in due diverse forme (isomeri) a livello molecolare. La differenza sta nell'orientamento relativo degli spin nucleari dei due atomi di idrogeno. A seconda che gli spin siano allineati nella stessa direzione o in quella opposta, uno si riferisce a orto- o para-acqua.
Esperimenti con molecole d'acqua selezionate
Il gruppo di ricerca guidato dal professor Stefan Willitsch del Dipartimento di Chimica dell'Università di Basilea ha studiato come le due forme di acqua differiscano in termini di reattività chimica, la loro capacità di subire una reazione chimica. Entrambi gli isomeri hanno proprietà fisiche quasi identiche, il che rende particolarmente difficile la loro separazione.
Questa separazione è stata resa possibile da un metodo basato sui campi elettrici sviluppato dal professor Jochen Küpper del Centro di Amburgo per la scienza del laser a elettroni liberi. Utilizzando questo approccio, i ricercatori sono stati in grado di avviare reazioni controllate tra gli isomeri dell'acqua "pre-ordinati" e gli ioni diazenilio ultrafreddi ("azoto protonato") tenuti in una trappola. Durante questo processo, uno ione diazenilio trasferisce il suo protone a una molecola d'acqua. Questa reazione si osserva anche nella chimica dello spazio interstellare.
Maggiore reattività
È stato dimostrato che la para-acqua reagisce circa il 25% più velocemente dell'orto-acqua. Questo effetto può essere spiegato in termini di spin nucleare che influenza anche la rotazione delle molecole d'acqua. Di conseguenza, diverse forze attrattive agiscono tra i partner di reazione. Para-acqua è in grado di attrarre il suo partner di reazione più fortemente dell'orto-forma, che porta ad una maggiore reattività chimica. Le simulazioni al computer hanno confermato questi risultati sperimentali.
Nei loro esperimenti, i ricercatori hanno lavorato con molecole a temperature molto basse vicine allo zero assoluto (circa -273°C). Queste sono le condizioni ideali per preparare con precisione i singoli stati quantistici e definire il contenuto energetico delle molecole, e per provocare una reazione controllata tra di loro. Willitsch spiega l'approccio sperimentale:"Meglio si possono controllare gli stati delle molecole coinvolte in una reazione chimica, meglio i meccanismi e le dinamiche sottostanti di una reazione possono essere studiati e compresi."