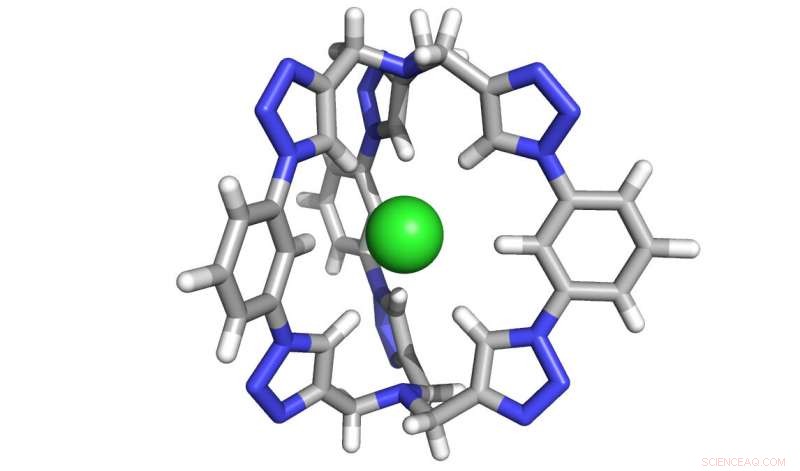
Un rendering al computer della gabbia di sei molecole di triazolo progettata per catturare i sali di cloruro. Credito:Yan Liu, Università dell'Illinois a Urbana-Champaign
I ricercatori dell'Università dell'Indiana hanno creato una nuova potente molecola per l'estrazione del sale dal liquido. Il lavoro ha il potenziale per contribuire ad aumentare la quantità di acqua potabile sulla Terra.
Costruito utilizzando legami chimici precedentemente considerati troppo deboli, la nuova molecola è circa dieci miliardi di volte migliorata rispetto a una struttura simile creata oltre 10 anni fa a IU. Il design delle molecole è stato riportato il 23 maggio sulla rivista Scienza .
"Se dovessi mettere un milionesimo di grammo di questa molecola in una tonnellata di acqua, Il 100% di loro sarà ancora in grado di catturare un sale, "ha detto Yun Liu, che ha guidato lo studio come Ph.D. studente nel laboratorio di Amar Flood, il James F. Jackson Professor di Chimica e Luther Dana Waterman Professor presso il Dipartimento di Chimica dell'IU Bloomington College of Arts and Sciences.
La molecola è progettata per catturare il cloruro, che si forma quando l'elemento cloro si accoppia con un altro elemento per ottenere un elettrone. Il sale cloruro più noto è il cloruro di sodio, o comune sale da cucina. Altri sali di cloruro sono cloruro di potassio, cloruro di calcio e cloruro di ammonio.
Mentre la popolazione umana continua a crescere, l'infiltrazione di sale nei sistemi di acqua dolce sta riducendo l'accesso all'acqua potabile in tutto il mondo. Solo negli Stati Uniti, l'US Geological Survey stima 271 tonnellate di solidi disciolti, compresi i sali, immettere corsi d'acqua dolce all'anno. I fattori che contribuiscono includono i processi chimici coinvolti nell'estrazione del petrolio, l'uso di sali stradali e addolcitori d'acqua, e l'erosione naturale della roccia. Basta un cucchiaino di sale per inquinare in modo permanente cinque litri d'acqua.
La nuova molecola di estrazione del sale creata a IU è composta da sei "motivi" triazolici:anelli a cinque membri composti da azoto, carbonio e idrogeno, che insieme formano una "gabbia" tridimensionale perfettamente sagomata per intrappolare il cloruro. Nel 2008, Il laboratorio di Flood ha creato una molecola bidimensionale, a forma di ciambella piatta, che usava quattro triazoli. I due triazoli extra conferiscono alla nuova molecola la sua forma tridimensionale, e dieci miliardi di volte in più di efficacia.
La molecola è anche unica perché lega il cloruro usando legami carbonio-idrogeno, precedentemente considerato troppo debole per creare interazioni stabili con il cloruro rispetto all'uso tradizionale dei legami azoto-idrogeno. Nonostante le aspettative, i ricercatori hanno scoperto che l'uso dei triazoli ha creato una gabbia così rigida da formare un vuoto al centro, che attira gli ioni cloruro.

Yun Liu tiene in mano un modello stampato in 3D della molecola di sei triazolo progettata per catturare i sali di cloruro. Credito:Fred Zwicky, Università dell'Illinois a Urbana Champaign.
Al contrario, le gabbie con legami azoto-idrogeno sono spesso più flessibili e il centro simile al vuoto necessario per la cattura del cloruro richiede un input di energia, riducendo la loro efficienza rispetto a una gabbia a base di triazolo.
"Se dovessi prendere la nostra molecola e impilarla contro altre gabbie che usano legami [più forti], stiamo parlando di molti ordini di grandezza di aumento delle prestazioni, " ha detto Flood. "Questo studio mostra davvero che la rigidità è sottovalutata nella progettazione di gabbie molecolari".
La rigidità consente inoltre alla molecola di mantenere la sua forma dopo la perdita del cloruro centrale, rispetto ad altri progetti che crollano nelle stesse circostanze a causa della loro flessibilità. Ciò fornisce alla molecola una maggiore efficacia e versatilità.
Il lavoro è anche riproducibile. La prima molecola ha impiegato quasi un anno per sintetizzare, disse Liu, che è rimasto scioccato nello scoprire i cristalli necessari per confermare la struttura unica della molecola formatasi dopo che l'esperimento è stato lasciato solo in laboratorio per diversi mesi, un evento sorprendente poiché questo processo richiede in genere un attento monitoraggio.
La formazione del cristallo ha rappresentato un momento "eureka", dimostrando che il design unico della molecola era effettivamente praticabile. Dopo, Wei Zhao, un ricercatore post-dottorato nel laboratorio di Flood, è stato in grado di ricreare la molecola in diversi mesi.