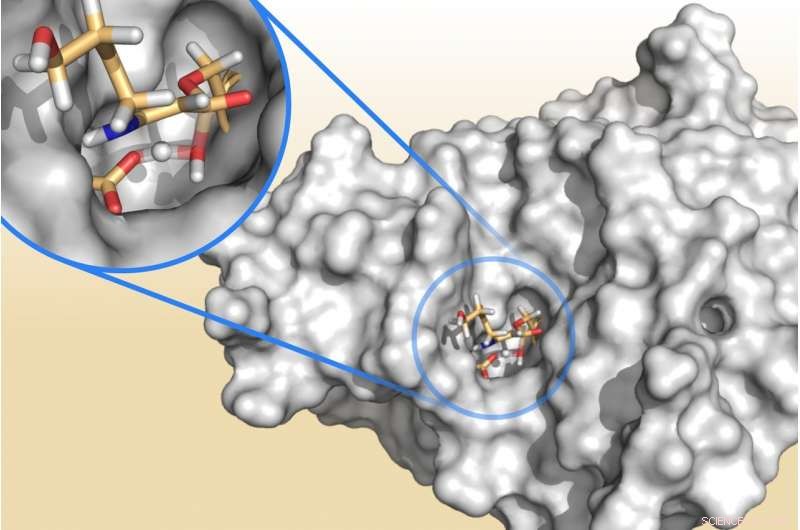
Un enzima batterico che rilascia frammenti di acido clavulanico, un "bloccante della resistenza" progettato per superare le infezioni resistenti agli antibiotici. La distruzione dell'acido clavulanico consente all'enzima di proteggere i batteri dagli effetti degli antibiotici. Credito:Marc van der Kamp
Attraverso simulazioni al computer, gli scienziati possono prevedere se i batteri possono essere fermati con terapie antibatteriche popolari o meno:una svolta che aiuterà a selezionare e sviluppare trattamenti efficaci per le infezioni batteriche.
La crescente resistenza agli antibiotici è una delle più gravi minacce per la salute globale che stiamo affrontando. C'è un urgente bisogno di sviluppare nuovi antibiotici che siano convenienti in quanto si stima che entro il 2050, 10 milioni di vite all'anno saranno a rischio di infezioni resistenti agli antibiotici. Nel tentativo di aiutare ad affrontare questa sfida, i ricercatori dell'Università di Bristol hanno sviluppato simulazioni al computer che potrebbero essere fondamentali per avanzare nella "corsa agli armamenti" in corso con i batteri.
I ricercatori si sono concentrati sugli enzimi nei batteri che possono dividere la struttura degli antibiotici di tipo penicillina, portando alla resistenza. Per ripristinare l'efficacia di questi antibiotici, Sono state sviluppate molecole di "blocco della resistenza" per bloccare l'attività di questi enzimi. Trattando i pazienti con le giuste combinazioni di antibiotici e bloccanti della resistenza, i medici sono in grado di prendere il sopravvento nella battaglia. Sfortunatamente, i batteri possono produrre molti enzimi diversi in grado di distruggere le penicilline, e i bloccanti della resistenza disponibili funzionano solo contro alcuni di questi.
Nuove scoperte, pubblicato in Biochimica , mostrano che ora è possibile utilizzare simulazioni al computer per prevedere se questi bloccanti della resistenza saranno efficaci o meno. Si spera che queste informazioni aiutino gli scienziati a sviluppare bloccanti della resistenza migliorati, che può ripristinare l'azione di antibiotici popolari contro una gamma più ampia di batteri resistenti.
Utilizzando una tecnica di simulazione al computer chiamata QM/MM (simulazioni di meccanica quantistica/meccanica molecolare), il team di ricerca di Bristol è stato in grado di ottenere informazioni a livello molecolare su come gli enzimi di resistenza reagiscono con i bloccanti della resistenza.
I ricercatori si sono concentrati specificamente sull'acido clavulanico, un farmaco che previene la distruzione dei comuni antibiotici simili alla penicillina. L'acido clavulanico è comunemente usato in combinazione con l'antibiotico amoxicillina per trattare l'orecchio, infezioni del seno e del tratto urinario (co-amoxiclav). Alcune di queste infezioni batteriche, però, stanno diventando molto più difficili da trattare perché l'acido clavulanico non funziona in modo efficace contro gli enzimi che producono.
Le simulazioni QM/MM hanno interrogato il modo in cui l'acido clavulanico interagisce con questi enzimi batterici e hanno rivelato il passaggio più importante nel determinare se l'enzima è effettivamente bloccato. Un enzima che non può essere fermato rilascia una molecola degradata di acido clavulanico e va a scomporre l'antibiotico con cui viene somministrato, con conseguente resistenza agli antibiotici. Se la degradazione dell'acido clavulanico richiede molto tempo, quindi l'enzima si "intasa" e non è in grado di abbattere l'antibiotico, che può quindi uccidere il batterio e cancellare l'infezione.
Dott. Marc van der Kamp, dalla Scuola di Biochimica dell'Università di Bristol, disse:
"Siamo entusiasti di vedere come le nostre simulazioni al computer possono essere utilizzate in futuro per testare gli enzimi dei batteri e prevedere quando un inibitore del blocco della resistenza sarà efficace.
Speriamo che questo identificherà come possiamo bloccare meglio tali enzimi batterici, in modo che gli antibiotici possano essere utilizzati efficacemente per il trattamento delle infezioni resistenti ai farmaci.
Le nostre simulazioni possono anche essere uno strumento prezioso per aiutare a scegliere quali combinazioni di farmaci sono le migliori per il trattamento di un particolare focolaio di infezione, permettendoci di essere meglio equipaggiati in questa "corsa agli armamenti" con i batteri".