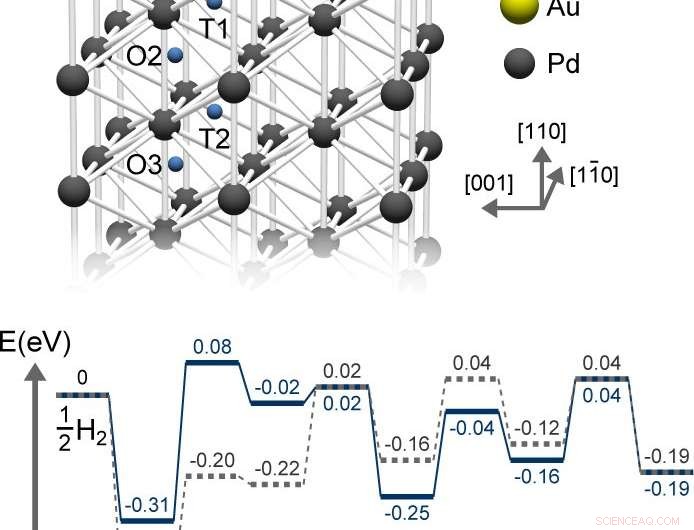
Gli atomi di Au destabilizzano l'idrogeno chemisorbito, aumentando così la loro energia e riducendo la barriera. Credito:2018 Shohei Ogura, Istituto di Scienze Industriali, L'Università di Tokyo
I materiali che assorbono l'idrogeno vengono utilizzati per lo stoccaggio e la purificazione dell'idrogeno, fungendo così da vettori di energia pulita. Il più noto assorbitore di idrogeno, palladio, può essere migliorato legandolo con l'oro.
Una nuova ricerca condotta dall'Istituto di scienze industriali dell'Università di Tokyo spiega per la prima volta come l'oro faccia una tale differenza, che sarà prezioso per mettere a punto ulteriori miglioramenti.
Il primo passo nello stoccaggio dell'idrogeno è il chemisorbimento, in cui l'H2 gassoso si scontra con il palladio e si adsorbe (si attacca) alla superficie. In secondo luogo, gli atomi di H chemisorbiti si diffondono nel sottosuolo, profondità di diversi nanometri. Un recente articolo pubblicato su Atti dell'Accademia Nazionale delle Scienze ( PNAS ) riferisce che il gruppo si è concentrato su questa lenta seconda fase, che è il collo di bottiglia del processo complessivo.
In palladio puro, solo circa 1 su 1, 000 delle molecole di H2 che si scontrano con il metallo assorbono effettivamente all'interno. Quindi, solo questi possono essere immagazzinati come vettori energetici. Però, quando la superficie del palladio è in lega con l'oro, l'assorbimento è oltre 40 volte più veloce.
È fondamentale ottenere la giusta quantità di oro:l'assorbimento di idrogeno è massimizzato quando il numero di atomi d'oro è leggermente inferiore alla metà (0,4) di un singolo monostrato di palladio, secondo lo studio. Questo è stato scoperto dalla spettroscopia di desorbimento termico, e dalla misurazione della profondità degli atomi di H utilizzando emissioni di raggi gamma.
"Volevamo sapere che ruolo ha l'oro, "Il primo autore dello studio Kazuhiro Namba dice. "Gli atomi d'oro sono per lo più sulla superficie della lega. Però, i nostri risultati hanno mostrato che lo stoccaggio dell'idrogeno è migliorato anche al di sotto di questa profondità, in palladio puro. Perciò, l'oro deve accelerare la diffusione dell'idrogeno nel sottosuolo, piuttosto che migliorarne la solubilità."
Questa diffusione agisce come una tipica reazione chimica:la sua velocità è determinata dalla barriera energetica, cioè l'ostacolo che gli atomi di H devono superare per penetrare nel palladio. L'altezza della barriera è il divario tra le energie degli atomi di H chemisorbiti e lo stato di transizione che devono attraversare per raggiungere il primo sito sotto la superficie.
Secondo i calcoli della teoria del funzionale della densità (DFT), gli atomi d'oro destabilizzano l'idrogeno chemisorbito, aumentando così la loro energia e riducendo la barriera. Rendendo la superficie un ambiente meno stabile per gli atomi di H, questo li incoraggia a penetrare più rapidamente in siti più profondi, invece di indugiare in superficie. La spettroscopia di fotoemissione suggerisce che gli atomi d'oro spingono l'energia degli elettroni di palladio verso il basso, indebolendo la loro capacità di chemisorbire idrogeno.
Però, gli atomi di H debolmente chemisorbiti hanno anche maggiori probabilità di desorbire semplicemente dalla superficie; cioè., tornare alla fase gassosa. Questo processo indesiderato spiega perché lo stoccaggio dell'idrogeno è massimizzato con solo 0,4 monostrati di oro:se viene aggiunto altro oro, il desorbimento dell'idrogeno supera la sua diffusione in palladio.
"Il nostro studio rivela, a livello elettronico, come la lega d'oro controlla l'assorbimento dell'idrogeno, ", afferma il coautore Shohei Ogura. "Questo ci aiuterà a progettare migliori materiali per lo stoccaggio dell'idrogeno, che svolgerà un ruolo nel trasporto di energia a emissioni zero, così come catalizzatori solidi per reazioni chimiche, che spesso dipendono dall'idrogeno legato alla superficie."