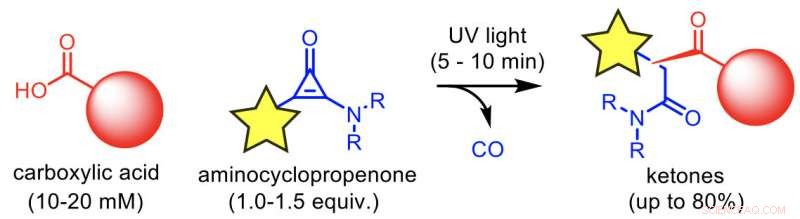
Modifica fotoattivata di un acido carbossilico utilizzando un aminociclopropenone. La reazione si completa in breve tempo (5-10 min) anche a bassa concentrazione (10-20 mM). La reazione di modifica procede con una resa fino all'80%. Credito:Università di Kanazawa
I ricercatori dell'Università di Kanazawa riferiscono nel Giornale di chimica organica che gli acidi carbossilici, gruppi funzionali contenuti nelle biomolecole, farmaci e materiali, può essere facilmente modificato da reazioni organiche indotte dalla luce utilizzando un aminociclopropenone. Questa scoperta apre nuove vie per la modifica dell'acido carbossilico con potenziali applicazioni tra cui la determinazione delle proteine bersaglio del farmaco, delucidazione della funzione delle proteine, e sintesi di materiali polimerici funzionalizzati.
Una reazione fotoinnescata è una reazione chimica indotta dall'irradiazione con la luce. Questa tecnica è utile per studi biochimici che mirano a ottenere una migliore comprensione della struttura e della funzione delle proteine, etichettandoli attraverso reazioni fotoinnescate. Un altro uso del metodo di reazione è la modifica dei polimeri. Ora, un team di ricercatori dell'Università di Kanazawa ha sviluppato una reazione di modifica fotoattivata di un acido carbossilico utilizzando un aminociclopropenone.
I ricercatori hanno precedentemente riferito sulla condensazione di disidratazione fotoattivata di un acido carbossilico e un'ammina utilizzando un aminociclopropenone. (Un acido carbossilico ha un gruppo COOH, con 'C' che denota carbonio, 'O' ossigeno e 'H' idrogeno. Un'ammina è una molecola organica con un atomo di azoto legato a tre sostituenti organici. Un aminociclopropenone è un composto organico con un anello di carbonio a tre membri sostituito con ossigeno e azoto.) L'irradiazione con luce debole fa sì che l'aminociclopropenone subisca la decarbonilazione per produrre una inammina altamente reattiva (una inammina è un composto organico che contiene un triplo C≡C legame sostituito con azoto). La ynamine risultante funziona come agente disidratante per collegare l'acido carbossilico e l'ammina.
Quando il team di ricerca ha studiato le condizioni dettagliate della condensazione di disidratazione fotoattivata, hanno scoperto che un'altra reazione si è verificata in condizioni di luce intensa. In questa reazione, è stata prodotta una miscela isomerica di tre chetoni (un chetone ha un doppio legame C=O, con due sostituenti attaccati all'atomo di carbonio). I chetoni hanno sostituenti derivati dall'acido carbossilico e dall'aminociclopropenone. In altre parole, l'acido carbossilico viene modificato con sostituenti sull'aminociclopropenone.
I ricercatori hanno ipotizzato che la reazione proceda attraverso i seguenti tre passaggi. (i) Un aminociclopropenone viene fotolizzato per produrre una inamina. (ii) Un acido carbossilico reagisce con la inamina per produrre un'acilossienamina. (Un'acilossienamina è un addotto 1:1 di un acido carbossilico e un'inamina.) (iii) L'acilossienamina viene fotolizzata per produrre una miscela isomerica di chetoni. I ricercatori hanno isolato l'intermedio dell'acilossienamina e ne hanno studiato le proprietà ottiche e la reattività chimica. I risultati dell'indagine hanno fortemente supportato l'ipotetico meccanismo.
Vari acidi carbossilici primari e secondari, inclusi derivati di amminoacidi, sono stati modificati con la reazione fotoattivata. In condizioni ottimizzate, i chetoni sono stati ottenuti con una resa combinata fino all'80%. Utilizzando un amminociclopropenone sostituito da un alchino terminale, il gruppo alchino è stato introdotto in un acido carbossilico (l'alchino presenta un triplo legame C≡C). Poiché vari gruppi funzionali possono essere introdotti selettivamente allo scaffold alchinico mediante la chimica click dell'alchino azide, un'ampia gamma di gruppi funzionali può essere introdotta in un acido carbossilico mediante la combinazione dell'introduzione dell'alchino fotoattivato e della reazione click dell'alchino azide. L'applicazione di questa reazione fotoattivata per modificare proteine e materiali è ora in fase di studio nel gruppo degli autori.