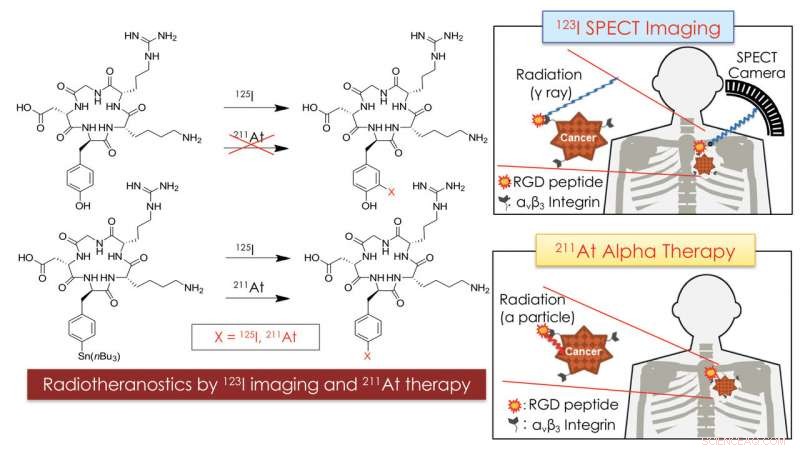
Il concetto di radioterapia che utilizza At-211 e I-123 per la diagnosi e la terapia del cancro. La combinazione dell'imaging SPECT utilizzando il peptide RGD marcato con I-123 con la terapia alfa mirata utilizzando il peptide RGD marcato con At-211 potrebbe essere utile per la medicina personalizzata contro il cancro. Credito:Università di Kanazawa
I ricercatori dell'Università di Kanazawa riferiscono in ACS Omega una promettente combinazione di molecole che trasportano radioisotopi per l'uso nella radioterapia:un approccio diagnostico e terapeutico basato sulla combinazione di imaging medico e radioterapia interna con elementi radioattivi.
Radioisotopi, atomi che mostrano radioattività, può essere utilizzato per la diagnosi e il trattamento del cancro. Per la diagnosi, radioisotopi che emettono raggi gamma sono utilizzati per la loro capacità di penetrazione, mentre per il trattamento, isotopi che emettono particelle alfa, particelle beta, o si utilizzano radiazioni citotossiche simili. La citotossicità si riferisce alla capacità di uccidere o danneggiare le cellule; in questo caso, cellule cancerogene.
Negli ultimi anni, un approccio che combina terapia e diagnosi basata su radioisotopi, chiamato radioteranostica, ha guadagnato trazione. L'idea chiave è che sia l'isotopo diagnostico che quello terapeutico possono essere somministrati a un tumore attaccandolo alla stessa molecola portatrice. Ora, Kazuma Ogawa dell'Università di Kanazawa e colleghi hanno sintetizzato un sistema radioteranostico con astato (At-211) come emettitore di particelle alfa e iodio (I-123) come fonte di radiazioni gamma.
Alcuni tipi di molecole possono essere utilizzati come vettori di radioisotopi. Ogawa e colleghi hanno utilizzato un peptide (una biomolecola costituita da una catena di amminoacidi) come vettore sia per l'astato che per l'isotopo di iodio. Nello specifico, hanno lavorato con un peptide contenente la cosiddetta sequenza di amminoacidi RGD. Il motivo RGD svolge un ruolo importante nel legame con la membrana cellulare; la sua attività adesiva cellulare lo rende un buon componente per la progettazione di molecole per colpire i tumori.
Le molecole carrier teranostiche sono state sintetizzate attraverso una serie di reazioni chimiche, l'ultimo passaggio è un'alogenazione, la sostituzione di un particolare componente molecolare con un alogeno. (Sia l'astato che lo iodio sono alogeni, aventi proprietà chimiche simili.)
Dopo la riuscita sintesi delle molecole carrier At-211 e I-125, i ricercatori hanno testato il loro comportamento in vivo. Hanno iniettato contemporaneamente i due composti in topi portatori di tumore, e osservò la biodistribuzione degli isotopi radioattivi, cioè, in quali parti del corpo si verificano, e quanto abbondantemente. La scoperta principale è stata che i peptidi RGD marcati con At-211 e I-125 hanno mostrato biodistribuzioni molto simili, con un alto accumulo nel tumore, un prerequisito per operare come un sistema teranostico. (Un altro isotopo di iodio, I-123, dovrebbe essere il radioisotopo diagnostico, ma I-125 ha un'emivita molto più lunga, rendendo più facile lavorare con i presenti esperimenti.)
Il lavoro di Ogawa e colleghi è un importante passo avanti nello sviluppo della radioterapia. Citando gli scienziati:"Questo metodo potrebbe essere applicabile ad altri peptidi direttamente mirati al cancro. Inoltre, gli sforzi futuri dovrebbero essere concentrati sull'applicazione di altri radioalogeni ... come emettitori di positroni per l'imaging PET [tomografia elettronica a positroni] ... "
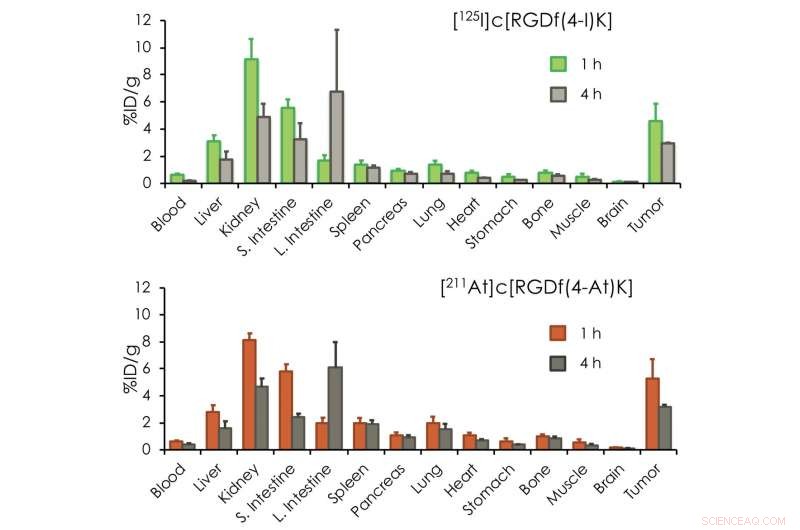
Biodistribuzione di [ 211 At]c[RGDf(4-At)K] e [ 125 I]c[RGDf(4-I)K] in topi portatori di tumore. [ 211 At]c[RGDf(4-At)K] e [ 125 I]c[RGDf(4-I)K] ha mostrato una biodistribuzione simile. Rende possibile la radioterapia. Credito:Università di Kanazawa