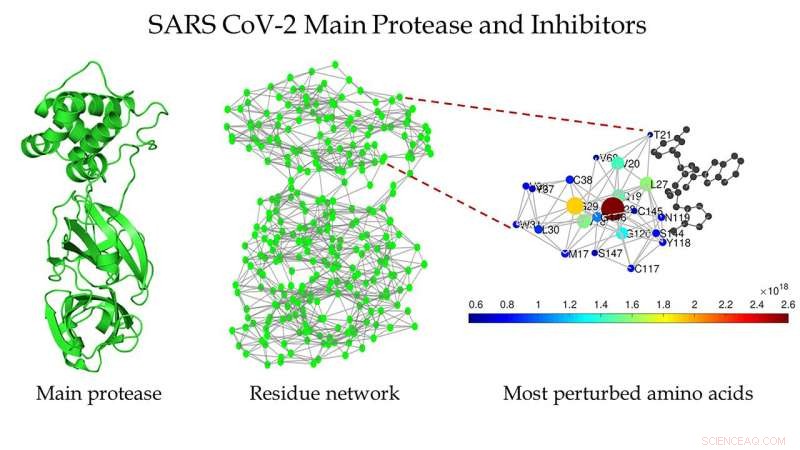
Schema della principale proteasi di SARS CoV-2 (a sinistra), la rete di residui proteici della principale proteasi di SARS CoV-2 (al centro), e una vista ingrandita della regione attorno al sito di legame rilevata da Estrada (a destra). Credito:Ernesto Estrada
Mentre la pandemia di COVID-19 causata dal coronavirus SARS-CoV-2 continua a diffondersi in tutto il mondo, molti ricercatori stanno studiando modelli epidemiologici per prevederne la propagazione.
Però, Ernesto Estrada, un matematico ed esperto di sistemi complessi della Fondazione ARAID presso l'Università di Saragozza, ha deciso di concentrarsi sulla ricerca di bersagli all'interno di SARS-CoV-2 per nuovi farmaci da attaccare. Da lavori precedenti, sapeva che la principale proteasi del virus, un enzima responsabile del trattamento proteolitico delle poliproteine, è un ottimo obiettivo.
Nel diario Caos , Estrada ha detto quando lui e i suoi colleghi hanno scoperto un drammatico aumento della sensibilità della principale proteasi di SARS-CoV-2 a piccoli disturbi, li ha fatti sospettare che gli inibitori abbiano un ruolo nell'uccidere il virus.
Gli inibitori sono molecole organiche, droghe, o nuovi composti chimici che si attaccano al sito di legame di una proteasi per inibirne il lavoro. Un virus morirà senza un enzima proteolitico che lavora per esso.
"Ho notato che i chimici avevano già trovato alcuni potenti inibitori della principale proteasi di SARS-CoV-2, e che avevano risolto la struttura di questa proteina tramite cristallografia a raggi X, " ha detto. "È stato scioccante vedere che questa proteasi è molto simile a quella del coronavirus SARS, che ha prodotto le epidemie del 2003, SARS-CoV-1".
Quando i ricercatori hanno sovrapposto entrambe le strutture l'una sull'altra, combaciavano quasi perfettamente.
"Se allinei le sequenze di amminoacidi di entrambe le proteasi, ci sono solo 12 residui su 306 che non coincidono, "Estrada ha detto. "C'è qualcosa di nascosto dietro queste apparenti somiglianze tra le due proteasi? Possiamo imparare qualcosa da loro per migliorare la progettazione di farmaci contro il virus?"
Il gruppo di Estrada ha una vasta esperienza nell'analisi delle reti, come i social network, Internet, o catene alimentari tra specie all'interno di un ambiente e ha deciso di trattare una proteina come rete.
"Si chiamano reti di residui proteici, dove rappresentiamo ogni amminoacido come un nodo, e l'interazione tra due amminoacidi è rappresentata da un legame tra i due, " Lui ha spiegato.
Hanno trovato diverse strutture della principale proteasi di SARS CoV-1 e SARS CoV-2 che erano pulite, il che significa che non contengono mutazioni, ligandi, o solventi all'interno delle loro strutture. Hanno trasformato la loro struttura in reti di residui proteici.
Estrada ha affermato che la maggior parte delle misure di rete tradizionali ha rivelato che entrambe le strutture erano molto simili tra loro, qualcosa che la sua squadra già sapeva. "Ma un paio di anni fa, abbiamo sviluppato una misura matematica più sofisticata che ci consente di rilevare quanto lontano può essere propagata una perturbazione all'interno di una rete. Quel lavoro era di natura molto teorica, natura matematica, ma avevamo ipotizzato che potesse essere utile per lo studio delle proteine».
Così l'hanno messo alla prova. Ha rivelato che la proteasi di SARS-CoV-2 è 1, 900% più sensibile alla trasmissione di perturbazioni a lungo raggio rispetto alla proteasi di SARS-CoV-1.
"Ciò significa che quando una proteina viene perturbata, per esempio dall'acqua all'interno dell'ambiente intracellulare, tali perturbazioni sono trasmesse attraverso una rete di intraresidui che formano la struttura 3-D della proteina, " ha detto Estrada. "Se tale perturbazione viene prodotta attorno a un determinato amminoacido all'interno della proteasi di SARS-CoV-1, viene trasmesso solo attraverso un ambiente vicino a quell'aminoacido perturbato".
Ma se questa perturbazione si verifica in un amminoacido all'interno della proteasi di SARS-CoV-2, viene trasmesso a quasi tutta la rete, anche agli amminoacidi molto lontani.
"È notevole, perché significa che con piccole differenze strutturali la proteasi di SARS-CoV-2 è molto più efficace nelle comunicazioni intraresiduali, Estrada ha detto. "Dovrebbe essere molto più efficace nel fare il suo lavoro come un enzima proteolitico del virus. Il diavolo ha fatto un lavoro quasi perfetto qui, ma ha lasciato la porta aperta. Questa grande sensibilità della proteasi SARS-CoV-2 alle perturbazioni può essere il suo tallone d'Achille in relazione agli inibitori".
L'approccio del gruppo può essere utilizzato per protocolli di screening massicci per identificare potenti inibitori della proteasi principale SARS-CoV-2 e, di conseguenza, per lo sviluppo di nuovi farmaci per ucciderlo.