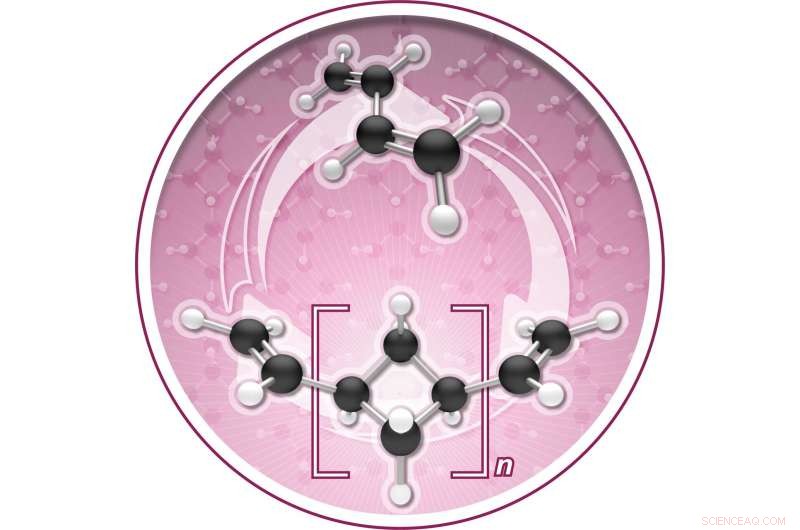
L'oligomerizzazione del butadiene catalizzata dal ferro [2+2] produce (1, n'-divinil)oligociclobutano, un nuovo polimero che può essere riciclato chimicamente. Credito:Jonathan Darmon del Dipartimento di Chimica dell'Università di Princeton.
Mentre il carico del pianeta di rifiuti di gomma e plastica aumenta senza sosta, gli scienziati guardano sempre più alla promessa del riciclaggio a ciclo chiuso per ridurre i rifiuti. Un team di ricercatori del Dipartimento di Chimica di Princeton annuncia la scoperta di una nuova molecola di polibutadiene, da un materiale noto da oltre un secolo e utilizzato per realizzare prodotti comuni come pneumatici e scarpe, che un giorno potrebbe far avanzare questo obiettivo attraverso la depolimerizzazione.
Il laboratorio Chirik riporta in Chimica della natura che durante la polimerizzazione la molecola, nominato (1, n'-divinil)oligociclobutano, incatena in una sequenza ripetuta di quadrati, una microstruttura precedentemente non realizzata che consente al processo di tornare indietro, o depolimerizzare, a determinate condizioni.
In altre parole, il butadiene può essere "zippato" per creare un nuovo polimero; quel polimero può quindi essere decompresso di nuovo in un monomero incontaminato per essere riutilizzato.
La ricerca è ancora in una fase iniziale e le caratteristiche prestazionali del materiale devono ancora essere esplorate a fondo. Ma il laboratorio Chirik ha fornito un precedente concettuale per una trasformazione chimica generalmente non ritenuta pratica per alcuni materiali di base.
Nel passato, la depolimerizzazione è stata realizzata con costosi polimeri di nicchia o specializzati e solo dopo una moltitudine di passaggi, ma mai da una materia prima comune come quella usata per fare il polibutadiene, uno dei primi sette prodotti petrolchimici primari al mondo. Il butadiene è un composto organico abbondante e un importante sottoprodotto dello sviluppo dei combustibili fossili. Viene utilizzato per realizzare prodotti in gomma sintetica e plastica.
"Prendere una sostanza chimica molto comune che le persone hanno studiato e polimerizzato per molti decenni e ricavarne un materiale fondamentalmente nuovo - per non parlare di quel materiale con interessanti proprietà innate - non solo è inaspettato, è davvero un grande passo avanti. Non ti aspetteresti necessariamente che ci siano ancora frutti su quell'albero, " ha detto Alex E. Carpenter, un chimico del personale con ExxonMobil Chemical, collaboratore della ricerca.
"Il focus di questa collaborazione per noi è stato lo sviluppo di nuovi materiali a beneficio della società concentrandosi su alcune nuove molecole che [il chimico di Princeton] Paul Chirk ha scoperto che sono piuttosto trasformative, " ha aggiunto il carpentiere.
"L'umanità è brava a produrre butadiene. È molto bello quando puoi trovare altre applicazioni utili per questa molecola, perché ne abbiamo in abbondanza".
Catalisi con Ferro
Il laboratorio Chirik esplora la chimica sostenibile studiando l'uso del ferro, un altro materiale naturale abbondante, come catalizzatore per sintetizzare nuove molecole. In questa particolare ricerca, il catalizzatore di ferro fa scattare insieme i monomeri di butadiene per produrre oligociclobutano. Ma lo fa in un motivo strutturale quadrato molto insolito. Normalmente, l'incatenamento avviene con una struttura a forma di S che è spesso descritta come simile a degli spaghetti.
Quindi, influenzare la depolimerizzazione, l'oligociclobutano è esposto al vuoto in presenza del catalizzatore di ferro, che inverte il processo e recupera il monomero. La carta del laboratorio di Chirik, "Sintesi catalizzata dal ferro e riciclaggio chimico di Telechelic, 1, Oligociclobutani 3-Enchained, " identifica questo come un raro esempio di riciclo chimico a ciclo chiuso.
Il materiale ha anche proprietà intriganti come caratterizzato da Megan Mohadjer Beromi, un borsista post-dottorato nel laboratorio Chirik, insieme ai chimici del centro di ricerca sui polimeri di ExxonMobil. Ad esempio, è telechelico, il che significa che la catena è funzionalizzata su entrambe le estremità. Questa proprietà potrebbe consentirne l'utilizzo come elemento costitutivo a sé stante, fungendo da ponte tra altre molecole in una catena polimerica. Inoltre, è termicamente stabile, il che significa che può essere riscaldato a oltre 250 gradi C senza una rapida decomposizione.
Finalmente, presenta elevata cristallinità, anche a basso peso molecolare 1, 000 grammi per mole (g/mol). Ciò potrebbe indicare che le proprietà fisiche desiderabili, come la cristallinità e la resistenza del materiale, possono essere ottenute con pesi inferiori rispetto a quanto generalmente ipotizzato. Il polietilene utilizzato nella media borsa della spesa di plastica, Per esempio, ha un peso molecolare di 500, 000 g/mol.
"Una delle cose che dimostriamo nel documento è che puoi realizzare materiali davvero resistenti da questo monomero, " ha detto Chirik, Edwards S. Sanford Professore di Chimica di Princeton. "L'energia tra polimero e monomero può essere vicina, e puoi andare avanti e indietro, ma ciò non significa che il polimero debba essere debole. Il polimero stesso è forte.
"Ciò che le persone tendono a pensare è che quando si dispone di un polimero riciclabile chimicamente, deve essere in qualche modo intrinsecamente debole o non durevole. Abbiamo fatto qualcosa che è davvero, molto resistente ma è anche riciclabile chimicamente. Possiamo recuperare il monomero puro. E questo mi ha sorpreso. Non è ottimizzato. Ma c'è. La chimica è pulita.
"Onestamente penso che questo lavoro sia una delle cose più importanti mai uscite dal mio laboratorio, " disse Chirik.
Abbandonare l'etilene
Il progetto risale a qualche anno fa, al 2017, quando C. Rose Kennedy, poi un postdoc nel laboratorio Chirik, notato un liquido viscoso che si accumula sul fondo di un pallone durante una reazione. Kennedy ha detto che si aspettava che si formasse qualcosa di volatile, quindi il risultato ha stimolato la sua curiosità. Scavando nella reazione, scoprì una distribuzione di oligomeri, o prodotti non volatili a basso peso molecolare, che indicava l'avvenuta polimerizzazione.
"Sapendo quello che sapevamo già del meccanismo, era abbastanza chiaro fin da subito come sarebbe stato possibile farli scattare insieme in modo diverso o continuo. Abbiamo immediatamente riconosciuto che questo potrebbe essere qualcosa di potenzialmente estremamente prezioso, " disse Kennedy, ora assistente professore di chimica presso l'Università di Rochester.
In quel primo momento, Kennedy stava incatenando butadiene ed etilene. Fu Mohadjer Beromi che in seguito ipotizzò che sarebbe stato possibile rimuovere del tutto l'etilene e utilizzare solo butadiene puro a temperature elevate. Mohadjer Beromi "ha dato" il butadiene a quattro atomi di carbonio al catalizzatore di ferro, e questo ha prodotto il nuovo polimero dei quadrati.
"Sapevamo che il motivo aveva la propensione ad essere riciclato chimicamente, " ha detto Mohadjer Beromi. "Ma penso che una delle nuove e davvero interessanti caratteristiche del catalizzatore di ferro sia che può fare [2+2] cicloaddizioni tra due dieni, ed è questo che essenzialmente è questa reazione:è una cicloaddizione in cui stai collegando due olefine insieme per creare una molecola quadrata più e più volte.
"È la cosa più bella su cui abbia mai lavorato in vita mia".
Per caratterizzare ulteriormente l'oligociclobutano e comprenderne le proprietà prestazionali, la molecola doveva essere ridimensionata e studiata in una struttura più grande con esperienza in nuovi materiali.
"Come fai a sapere cosa hai fatto?" Chirik ha chiesto. "Abbiamo usato alcuni dei normali strumenti che abbiamo qui in Frick. Ma ciò che conta davvero sono le proprietà fisiche di questo materiale, e infine come appare la catena."
Per quello, Chirik si è recato a Baytown, Texas l'anno scorso per presentare i risultati del laboratorio a ExxonMobil, che ha deciso di sostenere l'opera. Un team integrato di scienziati di Baytown è stato coinvolto nella modellazione computazionale, Lavoro di diffusione dei raggi X per convalidare la struttura, e ulteriori studi di caratterizzazione.
Riciclaggio 101
L'industria chimica utilizza un piccolo numero di elementi costitutivi per produrre la maggior parte delle materie prime di plastica e gomma. Tre di questi esempi sono l'etilene, propilene, e butadiene. Una delle principali sfide del riciclaggio di questi materiali è che spesso devono essere combinati e quindi rafforzati con altri additivi per produrre plastiche e gomme:gli additivi forniscono le proprietà prestazionali che desideriamo:la durezza di un tappo di dentifricio, Per esempio, o la leggerezza di una borsa della spesa. Questi "ingredienti" devono essere nuovamente separati nel processo di riciclaggio.
Ma i passaggi chimici coinvolti in quella separazione e l'apporto di energia necessaria per realizzarla rendono il riciclaggio proibitivo, in particolare per le plastiche monouso. La plastica è economica, leggero, e conveniente, ma non è stato progettato pensando allo smaltimento. Quella, disse Chirik, è il principale, problema valanga con esso.
Come possibile alternativa, la ricerca Chirik dimostra che il polimero butadiene è quasi energeticamente uguale al monomero, che lo rende un candidato per il riciclaggio chimico a ciclo chiuso.
I chimici paragonano il processo di produzione di un prodotto da una materia prima al rotolamento di un masso su una collina, con il picco della collina come stato di transizione. Da quello stato, fai rotolare il masso dall'altra parte e ti ritrovi con un prodotto. Ma con la maggior parte delle plastiche, l'energia e il costo per far rotolare quel masso all'indietro su per la collina per recuperare il suo monomero grezzo sono sbalorditivi, e quindi irrealistico. Così, la maggior parte dei sacchetti di plastica, dei prodotti in gomma e dei paraurti delle auto finisce nelle discariche.
"La cosa interessante di questa reazione di agganciare un'unità di butadiene alla successiva è che la 'destinazione' ha un'energia solo leggermente inferiore rispetto al materiale di partenza, " disse Kennedy. "Questo è ciò che rende possibile tornare indietro nella direzione opposta."
Nella fase successiva della ricerca, Chirik ha detto che il suo laboratorio si concentrerà sull'incatenamento, che a questo punto i chimici hanno raggiunto in media solo fino a 17 unità. A quella lunghezza di catena, il materiale diventa cristallino e così insolubile da cadere fuori dalla miscela di reazione.
"Dobbiamo imparare cosa fare con quello, " ha detto Chirik. "Siamo limitati dalla sua stessa forza. Mi piacerebbe vedere un peso molecolare più alto."
Ancora, i ricercatori sono entusiasti delle prospettive per l'oligociclobutano, e molte indagini sono previste in questa continua collaborazione verso materiali chimicamente riciclabili.
"L'attuale dotazione di materiali di cui disponiamo oggi non ci consente di avere soluzioni adeguate a tutti i problemi che stiamo cercando di risolvere, " ha detto Carpenter. "La convinzione è che, se fai una buona scienza e pubblichi su riviste peer-reviewed e lavori con scienziati di livello mondiale come Paul, poi questo permetterà alla nostra azienda di risolvere problemi importanti in modo costruttivo.
"Si tratta di capire una chimica davvero fantastica, " Ha aggiunto, "e cercando di fare qualcosa di buono con esso."