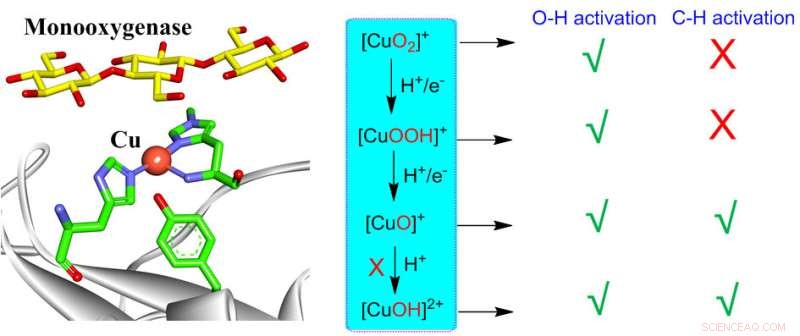
L'attivazione del diossido da parte del rame mononucleare nei sistemi biologici e sintetici può generare vari intermedi rame-ossigeno tra cui [CuO2 ] + , [CuOOH] + , [CuO] + , [CuOH] 2+ . Tutte queste specie sono in grado di eseguire l'attivazione O-H, mentre solo [CuO] + e [CuOH] 2+ sono reattivi per l'attivazione di CH. Tuttavia, la formazione di [CuOH] 2+ è altamente sfavorevole alle monoossigenasi, lasciando [CuO] + come unico intermedio attivo responsabile dell'attivazione di CH nelle monoossigenasi. Queste intuizioni possono fornire una comprensione coerente sulle reattività di varie specie attive rame-ossigeno nei sistemi biologici e sintetici. Credito:Giornale cinese di catalisi
Le attivazioni del diossigeno costituiscono uno dei problemi principali nei metalloenzimi rame-dipendenti. Su O2 attivazione, metalloenzimi rame-dipendenti, tra cui particolato metano-monoossigenasi (pMMO), polisaccaridi litici monoossigenasi (LPMO) ed enzimi binucleari del rame PHM e DBM, sono in grado di eseguire impegnative attivazioni del legame C-H/O-H.
Nel frattempo, i complessi contenenti nucleo rame-ossigeno sono stati sintetizzati per imitare le specie attive di metalloenzimi. L'attivazione del diossigeno da parte del sito attivo del rame mononucleare può generare intermedi rame-ossigeno, inclusi Cu(II)-superosso, Cu(II)-idroperosso, Cu(II)-ossile e le specie Cu(III)-idrossido.
È interessante notare che tutte queste specie sono state invocate come potenziali intermedi attivi per le attivazioni di CH/OH in sistemi biologici o sintetici. A causa della scarsa comprensione delle reattività del complesso rame-ossigeno, la natura delle specie attive nei sistemi sia biologici che sintetici è molto controversa.
Di recente, un gruppo di ricerca guidato dal Prof. Binju Wang dell'Università di Xiamen, in Cina, ha misurato le reattività di varie specie di rame-ossigeno mononucleate sia nei sistemi biologici che in quelli sintetici. Lo studio mostra:
Queste informazioni dovrebbero fornire una comprensione coerente sulle reattività di varie specie attive rame-ossigeno nei sistemi sia biologici che sintetici.
La recensione è stata pubblicata sul Chinese Journal of Catalysis . + Esplora ulteriormente