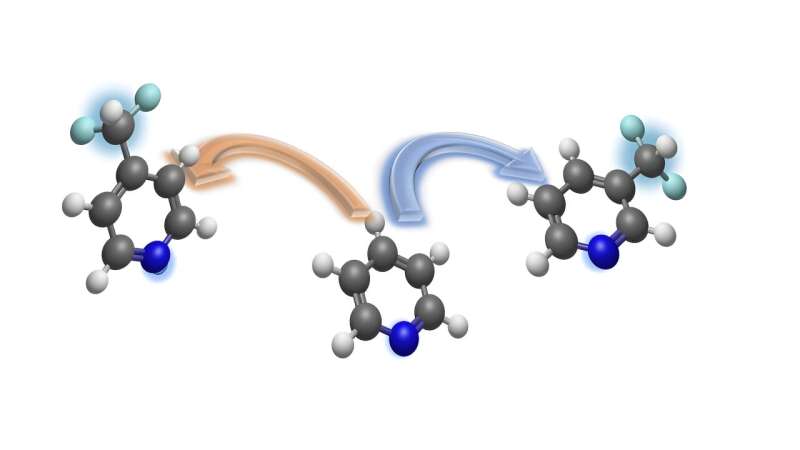
Un team di chimici dell'Università di Münster ha sviluppato un metodo di sintesi per l'integrazione selettiva del sito del gruppo difluorometilico biologicamente rilevante nelle piridine.
Il gruppo difluorometile determina spesso le proprietà delle molecole bioattive ed è quindi particolarmente interessante per la ricerca farmaceutica. Questo gruppo atomico è costituito da carbonio, due atomi di fluoro e un atomo di idrogeno. I derivati del composto chimico piridina sono particolarmente adatti per l'inclusione in gruppi difluorometilici.
Se un atomo di idrogeno nelle piridine viene sostituito da un tale gruppo, è possibile ottenere in modo semplice strutture ad anello difluorometilate, che sono potenziali candidati per nuovi farmaci e prodotti chimici per l'agricoltura. In termini di efficacia, la posizione del gruppo difluorometilico all'interno della molecola gioca un ruolo fondamentale.
Un team di ricercatori guidato dal Prof. Dr. Armido Studer dell'Istituto di chimica organica dell'Università di Münster (Germania) ha ora presentato una nuova strategia con la quale il gruppo difluorometile può essere introdotto con precisione nelle piridine in siti specifici. I risultati sono stati pubblicati sulla rivista Nature Communications.
La piridina è un elemento importante nell'industria farmaceutica e agrochimica per la produzione di sostanze biologicamente attive. La piridina e i suoi derivati contengono anelli con cinque atomi di carbonio e un atomo di azoto. Utilizzando il nuovo metodo, il gruppo difluorometile può essere introdotto nella posizione meta (a due atomi di distanza dall'azoto) o nella posizione para (a tre atomi di distanza dall'azoto).
Il metodo è promettente perché la difluorometilazione regioselettiva delle piridine è considerata una sfida nel campo della chimica. Non esistevano metodi precedentemente noti per la meta- e para-difluorometilazione selettiva del sito che potessero essere commutati tra le due posizioni. "Il nostro studio risolve il problema della difluorometilazione diretta dell'anello piridinico nella posizione meta, a cui è particolarmente difficile accedere nei composti complessi", spiega Studer.
Poiché le piridine sono composti piuttosto inerti, i chimici hanno applicato una strategia di dearomatizzazione temporanea. Gli intermedi attivi Dearomatizzati reagiscono con reagenti contenenti gruppi difluorometilici per formare le piridine chimicamente funzionalizzate. Questo metodo è adatto anche per la difluorometilazione di farmaci contenenti piridina alla fine della sequenza di sintesi. I derivati della piridina possono quindi essere facilmente convertiti invece di dover essere faticosamente ricostituiti.
"Il nostro metodo è pratico e può essere eseguito con reagenti poco costosi e disponibili in commercio. Ciò dovrebbe rendere il nostro metodo rilevante per la progettazione di farmaci", afferma il ricercatore post-dottorato Dr. Pengwei Xu. "Ci aspettiamo che il nostro approccio trovi applicazione nell'industria farmaceutica e agrochimica."
Ulteriori informazioni: Pengwei Xu et al, Introduzione del gruppo difluorometilico nella posizione meta o para delle piridine attraverso l'interruttore di regioselettività, Nature Communications (2024). DOI:10.1038/s41467-024-48383-1
Informazioni sul giornale: Comunicazioni sulla natura
Fornito dall'Università di Münster