I composti organici nel campo della chimica vanno da semplici idrocarburi a molecole complesse, con diversi gruppi funzionali aggiunti alla principale struttura del carbonio. Questi gruppi funzionali conferiscono proprietà chimiche distinte ai composti e partecipano a varie trasformazioni chimiche, rendendoli importanti precursori per la sintesi di composti più diversi. Gli scienziati si sono quindi impegnati attivamente nella creazione di molecole che presentano gruppi funzionali nuovi e altamente reattivi.
Una di queste classi di composti sono i dibenzotiofeni e i loro derivati contenenti porzioni di S-ossido o S,S-diossido (atomi di zolfo legati rispettivamente a uno e due atomi di ossigeno). Questi composti sono di particolare interesse nei campi delle scienze farmaceutiche, della chimica dei materiali e della biologia chimica.
I dibenzotiofeni sono costituiti da anelli di benzene fusi su un anello di tiofene, un anello a cinque membri con quattro atomi di carbonio e un atomo di zolfo. Quando gli S-ossidi di dibenzotiofene vengono esposti alla luce UV, rilasciano ossigeno atomico, utile per la scissione del DNA e l'ossidazione dell'adenosina-S'-fosfosolfato chinasi, un enzima coinvolto nei processi cellulari.
Inoltre, il legame S–O può essere attivato per introdurre diversi gruppi funzionali, consentendo la creazione di un’ampia gamma di molecole con proprietà e applicazioni diverse. Il metodo convenzionale per produrre ossidi S di dibenzotiofene funzionalizzati prevede la formazione di anelli di tiofene seguita dalla successiva S-ossidazione. Tuttavia, questa reazione è difficile da realizzare.
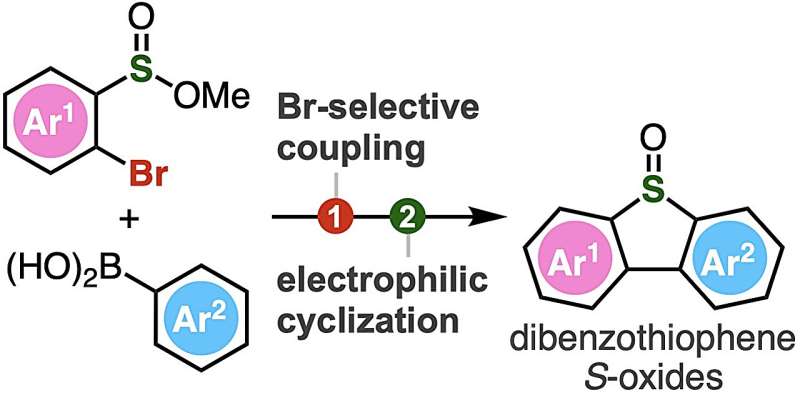
Per risolvere questo problema, il professore associato Suguru Yoshida, Yukiko Kumagai, Akihiro Kobayashi e Keisuke Nakamura dell'Università delle Scienze di Tokyo (TUS) hanno sviluppato un semplice metodo in due fasi per sintetizzare gli S-ossidi di dibenzotiofene. Il metodo prevede l'accoppiamento Suzuki-Miyaura di esteri solfinati 2-bromoaril sostituiti, seguito da una solfinilazione elettrofila intramolecolare.
I dettagli del metodo, pubblicati sulla rivista Chemical Communications il 10 gennaio 2024, apre la possibilità di creare una varietà di importanti molecole contenenti zolfo nelle scienze della vita che tradizionalmente erano difficili da sintetizzare utilizzando metodi convenzionali.
"Gli ossidi di dibenzotiofene stanno attirando l'attenzione nel campo della biologia chimica e diversi ricercatori hanno sviluppato una reazione utilizzando l'ossido di dibenzotiofene, che ora può essere sintetizzato utilizzando questo metodo. Ci aspettiamo che questa ricerca chiarisca i fenomeni vitali che coinvolgono le specie reattive dell'ossigeno", spiega Yoshida.
L'accoppiamento Suzuki-Miyaura è una reazione organica ampiamente utilizzata tra acidi boronici e alogenuri organici, che porta alla formazione di un nuovo legame carbonio-carbonio. Nel metodo proposto, gli esteri solfinati reagiscono prima con gli acidi arilboronici in presenza di un catalizzatore di palladio. Successivamente, i composti biarilici intermedi vengono attivati con Tf2 O, che porta alla successiva ciclizzazione per attivazione elettrofila.
Rispetto al metodo di ossidazione convenzionale per sintetizzare il dibenzotiofene, questo approccio innovativo sviluppato dal Dr. Yoshida e dal suo team può ospitare un'ampia gamma di gruppi funzionali, compresi quelli altamente reattivi, consentendo la sintesi di ossidi di dibenzotiofene polisostituiti non ottenibili prima.
Utilizzando il metodo, i ricercatori hanno sintetizzato ossidi di dibenzotiofene aventi una porzione o-sililaril triflato, un composto utile come sito di generazione di arine, ma che tende a danneggiarsi facilmente se prodotto utilizzando metodi convenzionali.
La porzione o-sililaril triflato funge da utile intermedio reattivo e può subire varie trasformazioni per produrre areni altamente sostituiti. Il metodo proposto, quindi, non solo semplifica il metodo di sintesi ma apre anche le porte a una vasta gamma di ossidi S di dibenzotiofene e loro derivati.
Il nuovo metodo rappresenta un significativo passo avanti nel campo della biologia chimica. Guardando al futuro, i ricercatori prevedono che questi composti potranno trovare utili applicazioni in diverse aree di ricerca, aprendo la strada a innovazioni e scoperte. "Il metodo proposto può consentire la sintesi di ossidi di benzotiofene polisostituiti, che dovrebbero essere utili in un'ampia gamma di campi di ricerca", conclude Yoshida.
Ulteriori informazioni: Yukiko Kumagai et al, Sintesi facile di dibenzotiofene S-ossidi da esteri solfinati, Comunicazioni chimiche (2024). DOI:10.1039/D3CC05703H
Informazioni sul giornale: Comunicazioni chimiche
Fornito dall'Università delle Scienze di Tokyo