I farmaci mirati mirano a individuare la posizione esatta nel corpo in cui si trova il tessuto malato e dove è necessario il medicinale. I molteplici vantaggi derivanti dalla somministrazione di un farmaco mirato includono una maggiore efficacia, poiché il farmaco è meticolosamente progettato per la specificità, riducendo così gli effetti collaterali e minimizzando i danni ai tessuti sani. Di conseguenza, questo approccio migliora la qualità della vita del paziente durante il trattamento.
Gli oligonucleotidi (ON), brevi catene di DNA o RNA appositamente progettate, sono emersi come uno strumento cruciale con un immenso potenziale nella medicina personalizzata. Questi ON terapeutici sono già in uso per condizioni, come alcuni tipi di distrofia muscolare e malattie del fegato, che i farmaci convenzionali non possono affrontare.
A seconda del tipo, gli ON possono funzionare prevenendo o modificando la produzione di una proteina nella cellula, particolarmente utile nelle malattie causate dalla sovrapproduzione di una proteina specifica.
Tuttavia, una sfida persistente risiede nel fornire con precisione ON terapeutici a una gamma più ampia di tessuti dove è necessario il trattamento delle cellule malate. I ricercatori hanno tentato di superare questo ostacolo attaccando piccoli marcatori proteici specifici a questi ON, noti come coniugati peptidici, riconoscibili dalle cellule malate.
Uno di questi peptidi è il peptide-1 simile al glucagone (GLP1), che è stato utilizzato per indirizzare specificamente gli ON terapeutici al pancreas. Questo peptide è l'analogo naturale del farmaco per il diabete e l'obesità Semaglutide venduto come Ozempic, Rybelsus e Wegovy.
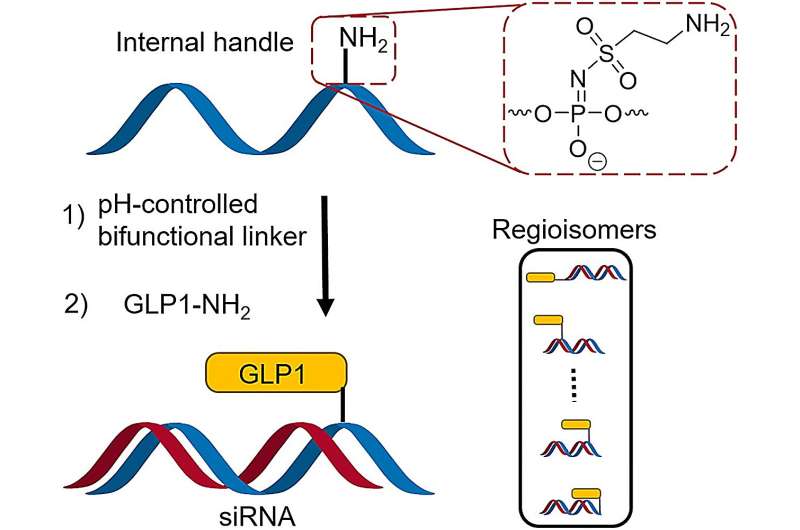
Il posizionamento delle modifiche chimiche sull'ON terapeutico è cruciale per il successo clinico di questa classe di farmaci. Allo stesso modo, il posizionamento del GLP1 nei coniugati peptide-ON potrebbe essere di assoluta importanza. Tuttavia, il posizionamento del ligando all'interno della sequenza ON ha, fino ad ora, richiesto componenti ON specializzati e costosi.
In stretta collaborazione con Novo Nordisk, il professor Kurt Gothelf e il suo gruppo di ricerca hanno ora ideato un metodo per semplificare la costruzione di un'intera libreria di coniugati ON-peptidici terapeutici. Come parte centrale della collaborazione, iNANO Ph.D. lo studente Jakob M. Smidt ha fatto visita allo specialista Lennart Lykke al Novo Nordisk a Måløv.
L'esperienza ha portato a una collaborazione di grande successo con nuove scoperte che sono vantaggiose per i ricercatori dell'industria farmaceutica e delle università. In questa collaborazione, i ricercatori hanno scoperto un metodo di sintesi per i coniugati ON che incorpora maniglie integrate e uno speciale linker, consentendo un facile collegamento degli ON a un marcatore peptidico regolando il pH.
L'aspetto degno di nota di questo metodo è l'eliminazione della necessità di elementi costitutivi ON specializzati e costosi per integrare i peptidi nella sequenza oligonucleotidica.
L'importanza di questo metodo risiede nella razionalizzazione del processo, rendendo la produzione di questi coniugati più accessibile ed economicamente vantaggiosa. Questa innovazione ha il potenziale per produrre ON terapeutici con molteplici funzioni, aprendo la strada a farmaci più efficaci.
Unendo l’esperienza nella chimica ON, inclusa la nuova tecnologia di funzionalizzazione, del laboratorio Gothelf insieme all’eredità scientifica dei peptidi di Novo Nordisk, è emersa una nuova e robusta chimica di coniugazione. Il metodo ha consentito di approfondire la relazione struttura-attività dei coniugati ON e rappresenta quindi un contributo scientifico molto importante alla comprensione di questa promettente classe di molecole terapeutiche.
Questo lavoro è il prodotto di una fruttuosa collaborazione pubblico-privato in cui conoscenze e nuove idee sono state apertamente condivise e discusse con l'ambizione comune di avere un impatto scientifico e potenzialmente fare la differenza per le persone che vivono con la malattia.
Gothelf immagina un futuro in cui questo metodo dirige i farmaci a base di ON verso tessuti specifici del corpo. Lo sviluppo di questo metodo segna un passo avanti significativo verso farmaci più efficaci e mirati, indicando il potenziale degli ON terapeutici personalizzati per somministrare farmaci esattamente nella posizione prevista nel corpo.
Ulteriori informazioni: Jakob Melgaard Smidt et al, Sintesi di coniugati peptide-siRNA tramite modifiche interne del sulfonilfosforamidato e valutazione della loro attività in vitro, Ricerca sugli acidi nucleici (2023). DOI:10.1093/nar/gkad1015
Informazioni sul giornale: Ricerca sugli acidi nucleici
Fornito dall'Università di Aarhus