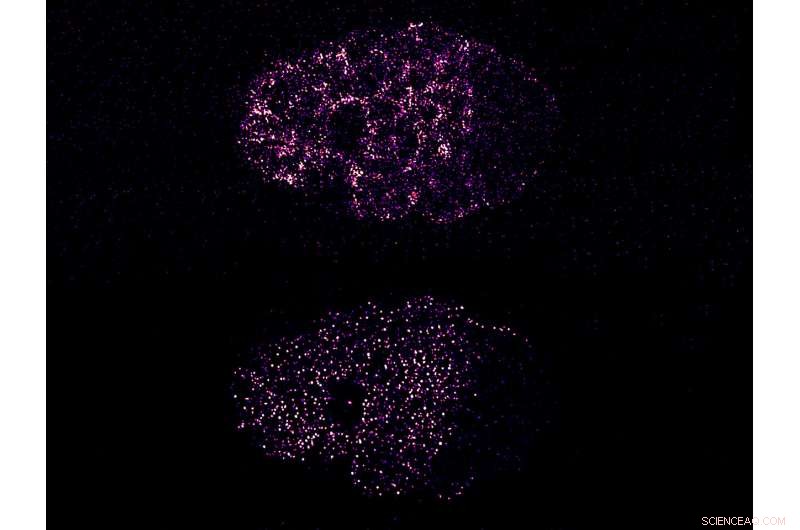
Figura:la contrazione guida il raggruppamento di proteine PAR per rompere la simmetria in un embrione di C. elegans. L'immagine in alto mostra l'attività contrattile della miosina corticale, che causa il raggruppamento della proteina PAR-3 (immagine in basso). Sia la miosina che il PAR-3 segregano sul lato sinistro dell'embrione, il polo anteriore. Questo rompe la precedente distribuzione simmetrica di queste proteine e polarizza la cellula. Credito:Istituto di Meccanobiologia, Singapore
Un team di ricercatori dell'Istituto di Meccanobiologia, Singapore (MBI) presso l'Università Nazionale di Singapore, insieme ai colleghi del Temasek Life Sciences Laboratory e dell'Istituto di biologia molecolare e cellulare di A*STAR a Singapore, ha scoperto un nuovo meccanismo per stabilire la polarità cellulare che si basa sul raggruppamento di proteine indotto dalla forza di tensione. Questo lavoro è stato pubblicato sulla rivista scientifica Biologia cellulare naturale nell'agosto 2017.
Le forze corticali inducono il raggruppamento proteico per la polarizzazione cellulare
Le cellule biologiche sono tipicamente visualizzate come di forma rotonda (o sferica), con un nucleo centrato nel mezzo, e altri componenti cellulari sparsi ovunque. In realtà, ogni tipo di cellula mostra una forma distinta, dimensione e composizione. Le rappresentazioni di sfere simmetriche è, in sostanza, una semplificazione eccessiva che nasconde il fatto che quasi tutte le cellule sono asimmetriche nella loro composizione, e che questa asimmetria si sviluppa in passaggi precisi e ben ordinati.
Conosciuto come polarità cellulare, questa caratteristica chiave delle cellule vede la separazione dei componenti subcellulari in regioni distinte della cellula. Se le cellule fossero simmetriche, processi come la divisione e il movimento delle cellule non avverrebbero correttamente, e tessuti e organi sarebbero deformati e non funzionanti. Nonostante sia parte integrante dello sviluppo dell'organismo, gli scienziati devono ancora definire completamente i processi attraverso i quali le cellule si polarizzano.
Un modo per visualizzare la natura asimmetrica della composizione cellulare è pensare ai componenti di un'auto e a come sono disposti. Alcune parti della vettura devono essere posizionate in un layout equilibrato, per esempio le ruote. Altri componenti devono essere disposti secondo un orientamento specifico per funzionare correttamente, cioè il sedile del conducente deve essere posizionato davanti ai sedili dei passeggeri posteriori. Finalmente, componenti come il motore possono essere posizionati nella parte anteriore o posteriore dell'auto, e soprattutto questa organizzazione impartisce proprietà diverse al trattamento dell'auto. Nello stesso modo, la disposizione dei componenti cellulari può avere effetti drastici sulla funzione cellulare.
Molti degli studi esistenti sulla polarità cellulare sono stati condotti nel verme nematode C. elegans. Allo stadio unicellulare, l'embrione si divide lungo un asse anteriore/posteriore per generare due cellule figlie di dimensioni diverse, con una cella più grande nella parte anteriore e una cella più piccola nella parte posteriore. Questo asse fronte/retro è stabilito dal movimento e dalla segregazione di un gruppo di proteine note come proteine PAR (partizione difettosa).
Queste proteine PAR risiedono nella corteccia cellulare, uno strato dinamico di filamenti proteici che si trova appena all'interno della membrana cellulare. Prima della polarizzazione, le proteine PAR sono distribuite in tutta la corteccia, dove si muovono liberamente. Durante la polarizzazione, la corteccia si contrae, e questo fa sì che diverse proteine PAR si separino e si accumulino nella parte anteriore o posteriore della cellula, rompendo così la loro organizzazione precedentemente simmetrica e stabilendo la polarità lungo l'asse anteriore/posteriore. Però, il meccanismo attraverso il quale l'attività contrattile trasporta e segrega le proteine PAR rimane poco chiaro.
Flusso di tensione
Il team di ricercatori guidato dall'assistente professore Fumio Motegi, Principal Investigator presso MBI e Temasek Life Sciences Laboratory, ha cercato di rispondere a questa domanda osservando il movimento dei complessi proteici PAR marcati con fluorescenza al microscopio in embrioni vivi di C. elegans mentre venivano sottoposti a polarizzazione. Utilizzando tecniche avanzate di microscopia, hanno scoperto che alcune proteine PAR assemblate in cluster all'inizio della polarizzazione, e questi ammassi crebbero di dimensioni man mano che la polarizzazione progrediva. Una volta interrotta la contrazione corticale, i grappoli smontati, con le proteine che si diffondono come un gradiente lungo l'asse anteriore/posteriore.
Nonostante questi riscontri, i ricercatori non hanno osservato una connessione diretta tra le fibre contrattili e le proteine PAR, e questo li ha portati a ipotizzare che un effetto indiretto di contrazione fosse responsabile del clustering. Interrompendo o rinforzando la corteccia dell'actomoisina e osservando l'effetto sulla formazione dei cluster, hanno scoperto che la forza chiave che guidava il raggruppamento PAR era la tensione corticale, che si sviluppa quando la corteccia si contrae.
Da questo i ricercatori sono stati in grado di proporre un nuovo modello che spiegasse la segregazione delle proteine PAR. Qui, la contrazione della corteccia dell'actomiosina porta ad un aumento della tensione corticale, provocando l'assemblaggio delle proteine PAR in cluster. Mentre questi grandi ammassi si muovono lentamente, vengono catturati nel flusso corticale complessivo e segregano a un'estremità della cellula, stabilendo così la polarità. Questi gruppi segregati di proteine PAR agiscono quindi come un'impalcatura che media un accumulo locale di altre proteine necessarie per la creazione di assi anteriore/posteriore lungo il corpo.
Il meccanismo scoperto in questo studio è un esempio semplice ma elegante di come le cellule utilizzino le forze interne per spostare e organizzare i loro componenti proteici in modo preciso, maniera ben ordinata. È importante sottolineare che il meccanismo guidato dalla forza descritto consente alla cellula di stabilire la polarità senza sprecare energia trasportando attivamente proteine o componenti cellulari contro un gradiente di concentrazione. Si ritiene che meccanismi simili vengano utilizzati per rompere la simmetria in altri organismi, compresi gli umani, e si spera che questa nuova conoscenza aiuterà gli scienziati a capire come e perché la polarità cellulare non viene stabilita correttamente in malattie come la fibrosi cistica e il cancro.