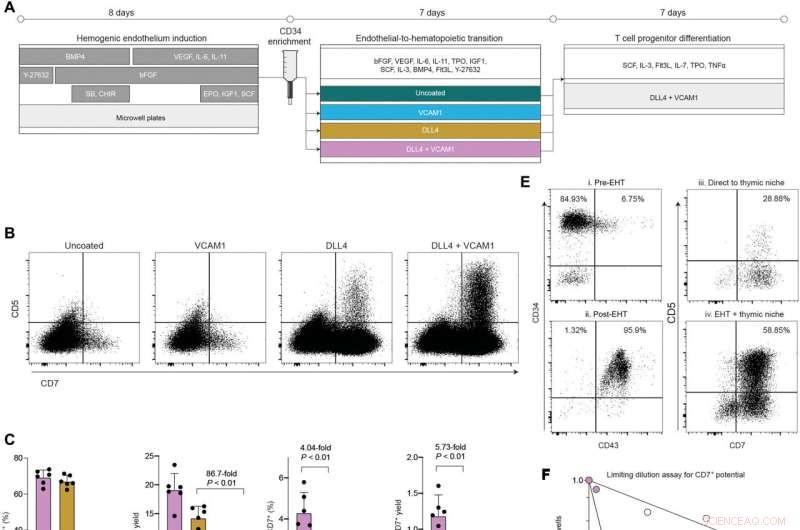
La presenza di DLL4 e VCAM1 durante la transizione endoteliale a ematopoietica supporta lo sviluppo di HSPC con un robusto potenziale di cellule T.(A ) Panoramica schematica della piattaforma chimicamente definita per la produzione di progenitori ematopoietici multipotenti e progenitori di cellule T da cellule staminali pluripotenti. (B ) Analisi della citometria a flusso dell'uscita dei linfociti T progenitori dopo la transizione delle cellule da 7 giorni in ciascuna condizione di rivestimento EHT in una nicchia timica definita comune per altri 7 giorni. (C ) Quantificazione della frequenza e della resa di CD7 + progenitori linfoidi e CD7 + , CD5 + Progenitori dei linfociti T dopo 7 giorni nella nicchia timica (media ± DS, n =6). Indicato P i valori riflettono il risultato del test di Mann-Whitney. (D ) Disegno sperimentale per valutare l'effetto dell'aggiunta o dell'omissione della fase di coltura EHT prima del trasferimento delle cellule nella nicchia timica. (E ) Immunofenotipo di cellule generate con o senza lo stadio di coltura EHT. I numeri in (E) corrispondono allo schema in (D). (V ) Risultati dell'analisi della diluizione limitante per valutare la frequenza delle cellule con CD7 + Potenziale linfoide NK/T all'interno del CD34 + popolazione con o senza un passaggio EHT. I numeri cellulari indicati sono stati seminati in piastre da 96 pozzetti e coltivati per un totale di 14 giorni (7 giorni EHT + 7 giorni di mezzo di differenziazione pro-T o 14 giorni di mezzo di differenziazione pro-T). I pozzi sono stati valutati come positivi se contenevano>25 CD7 + vitali cellule. Le frequenze sono state modellate come il numero di celle necessarie per raggiungere un tasso di fallimento di 0,37. (G ) Quantificazione della resa e della frequenza dei progenitori dei linfociti T generati con o senza una fase di coltura EHT. Indicato P il valore è per l'effetto di EHT su CD5 + , CD7 + resa, ANOVA a due vie. Credito:Progressi scientifici (2022). DOI:10.1126/sciadv.abn5522
Un team di ricerca dell'Università della Columbia Britannica ha sviluppato un nuovo processo rapido ed efficiente per la produzione di cellule immunitarie che combattono il cancro in laboratorio. La scoperta potrebbe aiutare a trasformare il campo della terapia cellulare immunitaria da uno sforzo costoso e di nicchia a qualcosa di facilmente scalabile e ampiamente applicabile.
"Abbiamo capito i passaggi minimi necessari per guidare in modo efficiente le cellule staminali pluripotenti a svilupparsi nella parabola in cellule immunitarie, in particolare le cellule T", ha affermato il dottor Yale Michaels, riferendosi alle cellule più essenziali del sistema immunitario umano. "Uno dei prossimi passi su cui stiamo lavorando è aumentare questo livello e farlo funzionare in modo più efficiente in modo da poter produrre abbastanza cellule per curare i pazienti".
Il documento rivoluzionario, pubblicato la scorsa settimana su Science Advances dal Dr. Michaels, Ph.D. lo studente John Edgar e un team del laboratorio del Dr. Peter Zandstra presso i Michael Smith Laboratories and School of Biomedical Engineering della UBC, descrivono un nuovo metodo che ora è il modo più veloce conosciuto per produrre cellule T in laboratorio.
Le cellule T sono fondamentali nella terapia CAR T, un trattamento del cancro ben noto e di successo che prevede l'ottenimento di cellule immunitarie dal paziente, modificandole geneticamente per combattere il cancro del paziente e reinfondendole nel corpo del paziente per combattere la malattia. Sebbene questo tipo di terapia abbia un tasso di efficacia vicino al 50 percento per alcuni tipi di cancro, è necessario creare un nuovo lotto di medicinali per ogni trattamento, che costa circa mezzo milione di dollari a turno.
"Poiché il costo principale associato a questi trattamenti è il fatto che sono realizzati individualmente, una strategia più conveniente potrebbe essere quella di capire come produrre quelle cellule immunitarie in laboratorio utilizzando le cellule staminali, invece di prenderle direttamente da un paziente ", spiega Michaels.
Le cellule staminali pluripotenti hanno la capacità di differenziarsi in qualsiasi tipo di cellula del corpo umano e possono rinnovarsi all'infinito. L'uso di PSC per creare cellule immunitarie in laboratorio per trattamenti terapeutici significa che centinaia di dosi di un medicinale potrebbero essere derivate da una singola cellula.
Basandosi su un ampio corpus di precedenti lavori nell'area, Michaels, Edgar e un team del laboratorio Zandstra hanno scoperto che la fornitura di due proteine alle cellule staminali durante una finestra chiave di sviluppo ha migliorato l'efficienza della produzione di cellule immunitarie di 80 volte. Lavorando rigorosamente con le proteine DLL4 e VCAM1, invece delle cellule animali e dei sieri che complicavano i metodi precedenti, il processo di produzione diventa una pipeline attentamente controllata che è facile da replicare.
Il miglioramento di questa pipeline di produzione è un passo tra i tanti verso la soluzione di una serie di sfide per la salute umana. Come aumentare un processo di differenziazione cellulare, come rendere le cellule in grado di uccidere il cancro e combattere altre malattie immunitarie e come fornirle ai pazienti in modo sicuro sono tutte questioni importanti che vengono esplorate simultaneamente dal laboratorio Zandstra e da altri gruppi di ricerca .
Il Dr. Michaels ha riconosciuto che il lavoro collettivo di migliaia di persone, ognuna delle quali ha dato un contributo importante, ha consentito a questo progetto di avere successo.
"Le persone hanno compiuto enormi progressi negli ultimi 20 anni e questa svolta è un continuum entusiasmante", ha affermato.
Il team spera che le loro nuove scoperte e il lavoro in corso in laboratorio contribuiranno alle future pipeline cliniche. + Esplora ulteriormente