I farmaci antibiotici sono diventati un trattamento popolare per le infezioni batteriche all’inizio del XX secolo e sono emersi come uno strumento di trasformazione nella salute umana. Durante la metà del secolo, durante l'epoca d'oro dei farmaci, furono regolarmente sviluppati nuovi antibiotici.
Ma poi i batteri si sono evoluti. Hanno trovato nuovi modi per eludere i trattamenti antibiotici, rendendone molti inutili. Man mano che le nuove fonti di antibiotici si esaurivano, le infezioni batteriche si sono intensificate fino all'attuale crisi sanitaria globale di resistenza agli antibiotici.
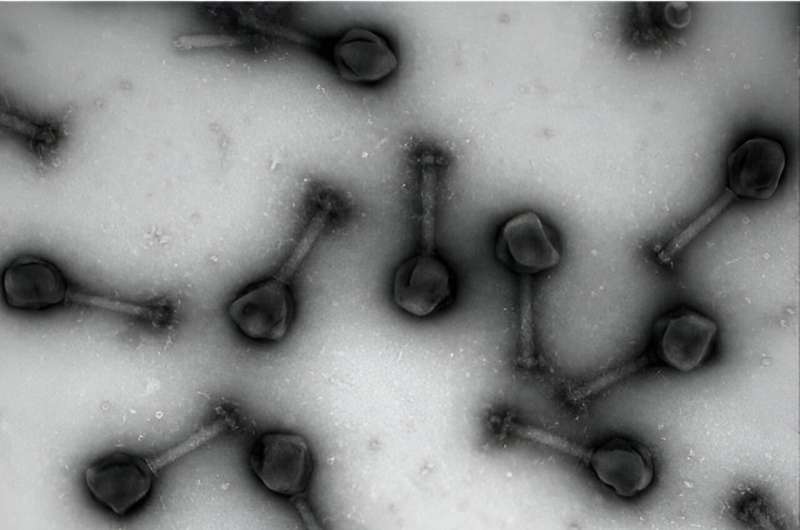
Gli scienziati ora guardano a un insolito alleato, i virus, per contribuire a contrastare questa crescente minaccia. Recentemente, i ricercatori si sono concentrati sui virus noti come batteriofagi come nuovo strumento per trattare e disarmare i batteri resistenti agli antibiotici. Un'attenzione particolare è stata posta sui fagi "jumbo" - virus recentemente scoperti che presentano genomi estremamente grandi - che potrebbero essere sfruttati come agenti di rilascio speciali che non solo possono uccidere i batteri ma potrebbero essere progettati per fornire antibiotici direttamente alla fonte dell'infezione.
Ma per fornire nuove terapie attraverso i fagi, gli scienziati devono prima comprendere la straordinaria composizione biologica e i meccanismi all'interno di questi misteriosi virus.
I ricercatori della San Diego School of Biological Sciences dell'Università della California e i loro colleghi dell'Innovative Genomics Institute della UC Berkeley e della Chulalongkorn University di Bangkok hanno compiuto un sostanziale passo avanti nella decifrazione di diverse funzioni chiave all'interno dei jumbofagi.
"Questi jumbo fagi hanno genomi di grandi dimensioni che in teoria potrebbero essere manipolati per trasportare carichi utili che uccidono in modo più efficace i batteri", ha detto Joe Pogliano, professore presso la School of Biological Sciences dell'UC San Diego e autore senior di un nuovo articolo pubblicato su Atti dell'Accademia Nazionale delle Scienze . "Il problema è che il loro genoma è racchiuso, quindi non è di facile accesso. Ma ora abbiamo scoperto alcuni dei suoi elementi chiave."
Come descritto nell'articolo, la ricerca condotta dallo studente laureato della School of Biological Sciences Chase Morgan si è concentrata sui fagi jumbo Chimalliviridae che si sono replicati all'interno dei batteri formando un compartimento che assomiglia al nucleo all'interno delle cellule degli esseri umani e di altri organismi viventi. Il compartimento simile al nucleo dei Chimalliviridae separa e importa selettivamente alcune proteine che gli consentono di replicarsi all'interno dei batteri ospiti. Ma il modo in cui si svolge questo processo è stata una parte sconcertante del processo.
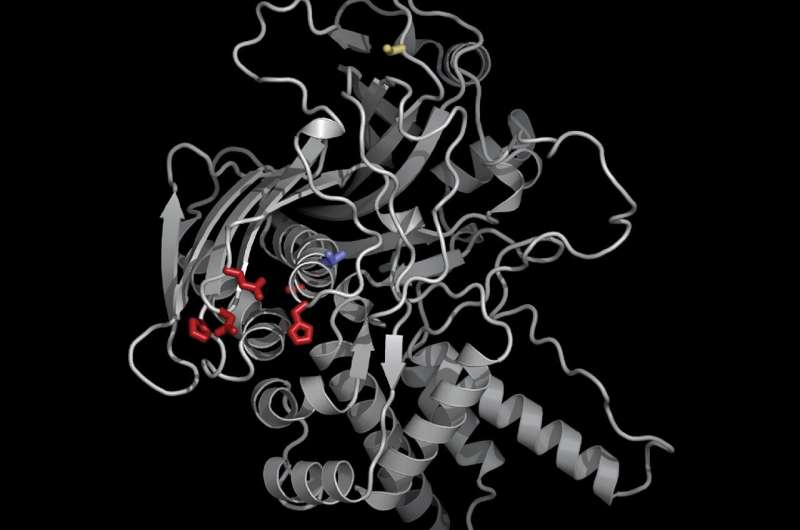
Utilizzando nuovi strumenti genetici e di biologia cellulare, Morgan e i suoi colleghi hanno identificato una proteina chiave, che hanno chiamato “importatore di proteine del Chimallivirus A” o PicA, che agisce come una sorta di buttafuori da nightclub, trafficando selettivamente le proteine garantendo l’ingresso all’interno del nucleo per alcuni ma negando l'accesso ad altri. Hanno scoperto che PicA coordina il traffico di proteine cargo attraverso il guscio protettivo del nucleo del fago.
"Solo il fatto che questo virus sia in grado di creare una struttura e un sistema di trasporto incredibilmente complessi è davvero sorprendente e non abbiamo mai visto prima", ha affermato Morgan. "Ciò che consideriamo biologia complessa è solitamente riservata a forme di vita superiori con gli esseri umani e le nostre decine di migliaia di geni, ma qui stiamo vedendo processi funzionalmente analoghi in un genoma virale relativamente piccolo di soli circa 300 geni. È probabilmente il metodo selettivo più semplice sistema di trasporto che conosciamo."
Utilizzando CRISPRi-ART, uno strumento di RNA programmabile per lo studio dei genomi, i ricercatori sono stati in grado di dimostrare che PicA è un componente essenziale del processo di sviluppo e replicazione del nucleo di Chimalliviridae.
"Senza la semplicità e la versatilità delle tecnologie CRISPR mirate all'RNA, porre direttamente queste domande e rispondere sarebbe quasi impossibile. Siamo davvero entusiasti di vedere come questi strumenti sveleranno i misteri codificati dai genomi dei fagi", ha affermato il coautore Ben Adler, un ricercatore. studioso post-dottorato che lavora con la pioniera del CRISPR, vincitrice del premio Nobel, Jennifer Doudna.
Batteri e virus sono impegnati in una sorta di corsa agli armamenti da miliardi di anni, evolvendosi ciascuno per contrastare gli adattamenti degli altri. I ricercatori affermano che il sofisticato sistema di trasporto PicA è il risultato di questa intensa e continua competizione evolutiva. Il sistema si è evoluto per essere altamente flessibile e altamente selettivo, consentendo solo gli elementi benefici chiave all’interno del nucleo. Senza il sistema PicA, le proteine difensive dei batteri riuscirebbero a penetrare all'interno sabotando il processo di replicazione del virus.
Tali informazioni sono fondamentali poiché gli scienziati dell'Emerging Pathogens Initiative e del Center for Innovative Phage Applications and Therapeutics dell'UC San Diego si sforzano di gettare le basi per programmare geneticamente i fagi per curare una varietà di malattie mortali.
"In realtà non avevamo alcuna comprensione di come funzionasse il sistema di importazione delle proteine o di quali proteine fossero coinvolte in precedenza, quindi questa ricerca è il primo passo nella comprensione di un processo chiave che è fondamentale affinché questi fagi si replichino con successo", ha affermato la School of Biological Sciences. la studentessa laureata Emily Armbruster, coautrice dell'articolo. "Più comprendiamo questi sistemi essenziali, meglio saremo in grado di progettare i fagi per uso terapeutico."
I futuri obiettivi di tali virus geneticamente programmati includono i batteri Pseudomonas aeruginosa, noti per causare infezioni potenzialmente fatali e comportare rischi per i pazienti negli ospedali. Altri bersagli promettenti includono E. coli e Klebsiella che possono causare infezioni croniche e ricorrenti e, in alcuni casi, entrare nel flusso sanguigno mettendo a rischio la vita.
Ulteriori informazioni: Chase J. Morgan et al, Un percorso di importazione di proteine essenziale e altamente selettivo codificato dal fago che forma nucleo, Atti dell'Accademia nazionale delle scienze (2024). DOI:10.1073/pnas.2321190121
Informazioni sul giornale: Atti dell'Accademia Nazionale delle Scienze
Fornito dall'Università della California - San Diego