La specie attiva nella reazione catalitica che esce sulla superficie fusa del tungstato di sodio è il perossido di sodio. Riprodotto con il permesso di riferimento. Credito:Wiley-VCH Verlag GmbH &Co.
La superficie fusa di un materiale a base di sodio potrebbe favorire la conversione diretta del metano in utili elementi costitutivi.
Affinché il gas naturale possa essere convertito in modo efficiente in prodotti industriali utili, è necessario il giusto processo catalitico. I ricercatori di KAUST e degli Stati Uniti combinano tecniche all'avanguardia per la caratterizzazione dei materiali per dimostrare un percorso di reazione unico che dimostra che i catalizzatori fusi a base di sodio possono fornire tutte le specie chimiche necessarie per ottimizzare il processo.
I radicali liberi, molecole con un elettrone di valenza spaiato, come il radicale ossidrile, svolgono un ruolo cruciale nella conversione di importanza industriale del gas naturale, principalmente metano, all'etilene:un composto organico vitale che costituisce gli elementi costitutivi di molti prodotti e polimeri. Per potenziare questo processo, noto come accoppiamento ossidativo, è fondamentale sviluppare catalizzatori selettivi.
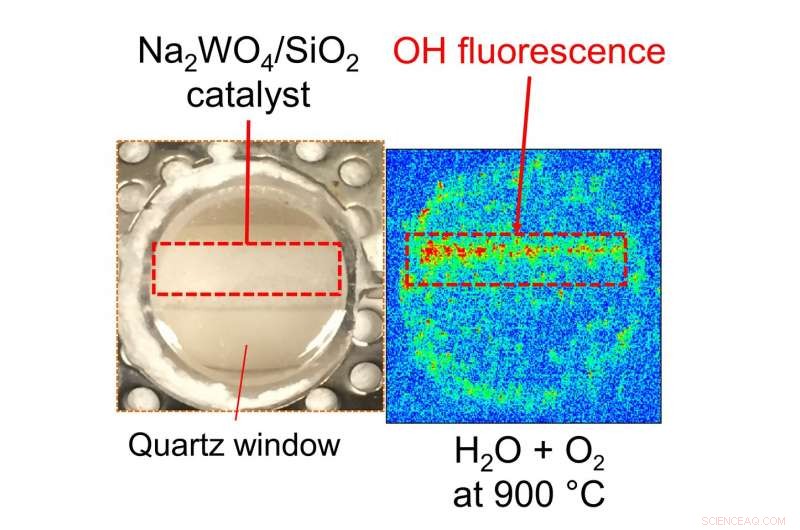
Il team KAUST, guidato da Kazuhiro Takanabe e dal suo studente Abdulaziz Khan, ha utilizzato strumenti in situ per misurare lo stato di un catalizzatore in condizioni di reazione. Hanno scoperto che le specie attive nella reazione catalitica che esce sulla superficie fusa del tungstato di sodio, una sostanza chimica necessaria per la reazione, è il perossido di sodio. Questo catalizzatore è unico in quanto invece di attivare direttamente il metano, attiva prima l'acqua e poi genera radicali ossidrili gassosi.
L'accoppiamento ossidativo del metano converte il metano e l'ossigeno in etilene in un singolo reattore. Precedenti ricerche nel laboratorio di Takanabe avevano indicato che utilizzando il tungstato di sodio a temperature superiori a 700 °C, la presenza di acqua può sia aumentare il tasso di conversione del metano sia aumentare la selettività del prodotto. Ciò potrebbe potenzialmente verificarsi tramite la formazione di radicali idrossilici e perossido di sodio, ma non c'erano prove dirette della presenza di queste specie.
Ora, Takanabe ei suoi coautori forniscono prove dirette della formazione di questi radicali liberi sulla superficie fusa del tungstato di sodio. Combinano una vasta gamma di tecniche sperimentali, compresa la diffrazione dei raggi X, microscopia elettronica della trasmissione di scansione, spettrometria di fluorescenza indotta da laser e spettroscopia fotoelettronica a raggi X, osservare uno strato esterno di tungstato di sodio fuso ricco di idrossido di sodio. "Abbiamo identificato esclusivamente la fase attiva del catalizzatore in uno stato unico in condizioni di reazione, " spiega Takanabe.
Ciò a sua volta conferma che un catalizzatore a base di sodio può formare radicali idrossilici da una miscela di ossigeno e acqua, una reazione mai vista. "Questo catalizzatore e l'esclusivo percorso di reazione hanno un grande potenziale per l'uso in varie reazioni catalitiche per la conversione del gas naturale, raffineria di petrolio e reazioni di combustione, "dice Takanabe.
Più in generale, questo successo dimostra anche l'importanza di combinare tecniche spettroscopiche e microscopiche in situ per comprendere meglio la chimica in fase gassosa ad alta temperatura.