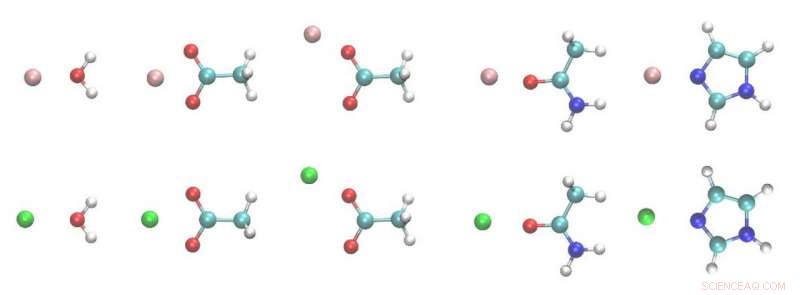
Strutture dei dimeri metallo ione-ligando. Bianco, ciano, blu, rosso, le sfere rosa e verdi sono H, C, N, Oh, Atomi di Mg e Ca. Credito:Zhifeng Jing, Rui Qi, Chengwen Liu e Pengyu Ren
Contrazioni muscolari, digestione del lattosio, circolazione sanguigna:cosa potrebbe collegare queste funzioni del corpo? Potresti essere sorpreso di apprendere che tutti questi processi e molti altri sono guidati da ioni metallici.
Sodio (Na+), potassio (K+), calcio (Ca2+) e magnesio (Mg2+) potrebbero essere nomi familiari, ma sono anche fondamentali per la funzione delle cellule umane. La combinazione di questi ioni con le proteine corporee crea complessi che sono indispensabili per la nostra continua esistenza.
L'importanza delle interazioni tra proteine e ioni metallici è ben compresa, ma le interazioni meccanicistiche tra i due sono ancora lontane dall'essere un quadro completo.
Zhifeng Jine, Rui Qi, Chengwen Liu e Pengyu Ren, professori del dipartimento di ingegneria biomedica dell'Università del Texas ad Austin, stanno lavorando per descrivere quantitativamente le interazioni proteina-ione utilizzando quello che viene chiamato un campo di forza energetico ottimizzato multipolare atomico per applicazioni biomolecolari (AMOEBA). Descrivono il loro lavoro nel di questa settimana Giornale di Fisica Chimica .
La tecnologia AMOEBA è stata sviluppata da Ren e Jay Ponder, dell'Università del Texas ad Austin e della Washington University di St. Louis. Utilizza un modello multipolare atomico polarizzabile per calcolare l'energia potenziale di un sistema. Il modello AMOEBA mira ad affrontare le inadeguatezze note dell'attuale tecnologia del campo di forza per modellare accuratamente le interazioni di ioni e proteine.
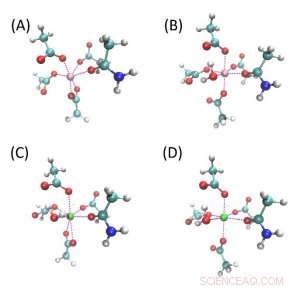
Strutture di composti modello per tasche a legame ionico. (A) e (B) sono tasche per legare Mg mentre (C) e (D) sono tasche per legare Ca. Bianco, ciano, blu, rosso, le sfere rosa e verdi sono H, C, N, Oh, Atomi di Mg e Ca. Tutte queste quattro strutture sono costituite da quattro molecole di acetato e una acetamide, e (B-D) hanno una molecola d'acqua aggiuntiva. (A) e (C) hanno ciascuno un acetato bidentato, e tutto l'altro acetato si lega allo ione metallico con un atomo di ossigeno. Questi quattro modelli sono indicati come Mg-Bi, Mg-Mono, Ca-Bi e Ca-Mono rispettivamente. Credito:Zhifeng Jing, Rui Qi, Chengwen Liu e Pengyu Ren
"La mancanza di una comprensione dettagliata è principalmente dovuta alla mancanza di modelli accurati e tuttavia efficienti dal punto di vista computazionale per trattare gli ioni metallici, Ren ha detto. "Il nostro obiettivo è applicare metodi di meccanica quantistica di alto livello e simulazioni avanzate del campo di forza per comprendere la natura delle interazioni tra ioni metallici e proteine".
AMOEBA migliora le simulazioni biomolecolari classiche, i cui modelli rappresentano l'interazione intermolecolare utilizzando la somma di due forze, secondo Ren:l'interazione di van der Waals e l'interazione di Coulomb tra cariche puntiformi.
"Questa rappresentazione è abbastanza semplice da essere trattabile computazionalmente, ed è stato ampiamente utilizzato negli ultimi decenni, " ha detto. "Tuttavia, ioni metallici possono portare a forti effetti di polarizzazione e trasferimento di carica, che mancano in questi modelli classici. Riteniamo che questi effetti svolgano un ruolo critico nell'interazione specifica ione-proteina".
Ren e i suoi colleghi hanno esaminato specificamente l'interazione di Mg2+/Ca2+ e amminoacidi. Il magnesio e il calcio sono alcuni degli ioni più abbondanti nelle metalloproteine, proteine con un cofattore di ioni metallici. Entrambi sono selettivamente legati a specifici aminoacidi, rendendole interessanti molecole bersaglio. La risposta a molti corpi, l'induzione reciproca tra ioni e i loro residui circostanti all'interno delle tasche di legame proteico, influisce anche sull'affinità di legame di questi ioni e può essere catturato dal modello AMOEBA.
"La differenza tra la risposta di molti corpi al Ca2+ rispetto al Mg2+ nella tasca di rilegatura è sostanziale, " ha detto Ren. "Si sapeva che la polarizzazione e il trasferimento di carica sono importanti nei complessi proteina-ione, ma per il legame competitivo, molti hanno sospettato che questi effetti potessero annullarsi".
Il modello AMOEBA e gli avanzamenti dei campi di forza, comprese le applicazioni di questi risultati, Ren ha sottolineato, sono rilevanti in molte malattie tra cui il cancro e le malattie neurodegenerative. La conoscenza delle interazioni proteina-ione può fornire una comprensione fondamentale per il progresso nelle ricerche mediche correlate.