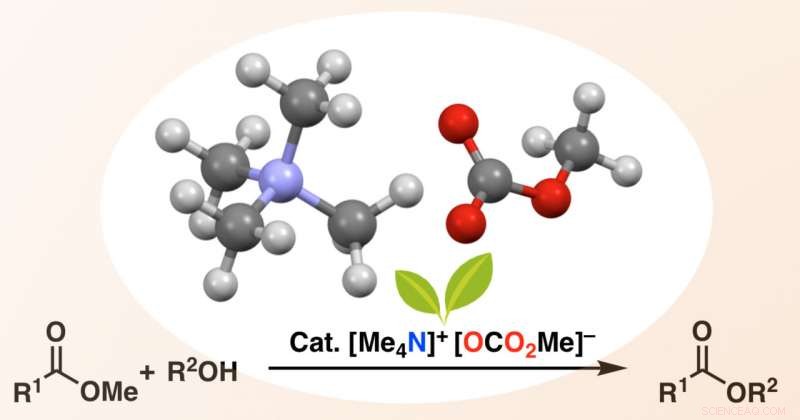
Il tetrametilammonio metil carbonato (TMC) reagisce in situ con un alcol per formare uno ione alcossido, che poi attacca l'estere di partenza per dare il complesso estere bersaglio in alte rese. Credito:Manabu Hatano &Kazuaki Ishihara
Gli esteri sono tra le classi più importanti di composti in chimica organica. Gli esteri semplici sono noti per la loro piacevolezza, aromi spesso fruttati. Nel frattempo, il più grande, esempi più complessi hanno un ampio spettro di usi industriali, che vanno da lenti e creme idratanti al carburante "verde" (biodiesel).
Un modo comune per produrre esteri complessi è far reagire esteri carbossilici più semplici con alcoli. Conosciuto come trans-esterificazione, questo processo si basa tipicamente su sali metallici come catalizzatori. Però, tali catalizzatori tendono ad essere costosi e/o inquinanti. Ancora peggio, se l'estere è lungo e flessibile, tende ad avvolgere il centro metallico attraverso legami di coordinazione. Legando efficacemente il metallo, questa "chelazione" spegne la reazione.
Ora, un team dell'Università di Nagoya ha sviluppato un catalizzatore che espande notevolmente la gamma di substrati della trans-esterificazione. Per evitare la chelazione, i ricercatori hanno utilizzato un catalizzatore privo di metalli, tetrametilammonio metil carbonato (TMC). Nelle giuste condizioni, TMC reagisce in situ con un alcol per formare uno ione alcossido, che poi attacca l'estere di partenza per dare il complesso estere bersaglio in alte rese.
Secondo Manabu Hatano, coautore dello studio del team in Chimica verde , questo non è il primo processo che utilizza alcossidi per la transesterificazione, ma è di gran lunga il più versatile. "Gli sforzi precedenti hanno utilizzato sali di fosfonio, ma l'alcossido risultante può esterificare solo il solvente stesso, che deve essere dimetilcarbonato (DMC). Va bene se vuoi un prodotto che può essere derivato da DMC, ma per il resto hai bisogno di sali che siano stabili in solventi più convenzionali. La nostra nuova TMC colma questa lacuna."
La gamma di alcoli ed esteri che possono essere combinati utilizzando TMC è davvero ampia. Possono partecipare amminoalcoli, anche se il gruppo amminico disattiverebbe i tipici catalizzatori metallici per chelazione. È stato anche costruito un derivato del chinino con un anello a ponte 3-D sul lato alcolico. Nel frattempo, tra i substrati esteri, gli esteri degli amminoacidi chirali possono essere reagiti con successo, e la purezza dell'enantiomero corretto è preservata in modo sicuro. Come i precedenti sali di fosfonio, il nuovo catalizzatore può essere utilizzato anche per esterificare il solvente stesso, che consente di risparmiare denaro quando il solvente è in viaggio verso l'obiettivo.
"Essendo sia riciclabile che privo di metalli, questo catalizzatore è un vero esempio di chimica verde, " dice l'autore principale Kazuaki Ishihara. "Non solo il processo stesso è verde, ma possiamo usarlo per produrre biodiesel verde, che è una miscela di esteri. Abbiamo sintetizzato centinaia di grammi di uno dei principali componenti del biodiesel, che è abbastanza copioso per una reazione su scala di laboratorio. Questo ci dà fiducia che la reazione può essere scalata fino alla produzione industriale".