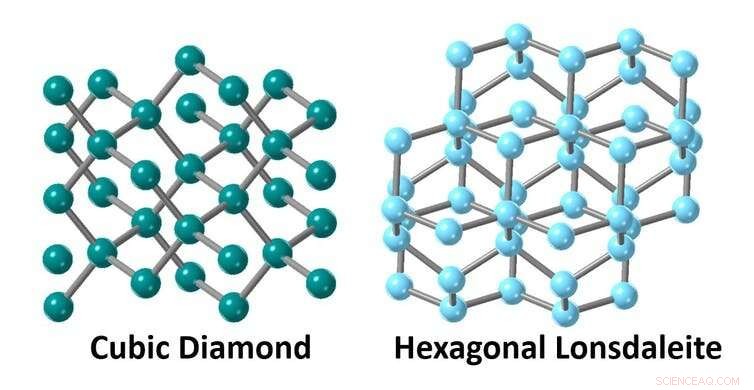
Le strutture cristalline del diamante cubico e della Lonsdaleite esagonale hanno atomi disposti in modo diverso.
In natura, i diamanti si formano nelle profondità della Terra per miliardi di anni. Questo processo richiede ambienti con pressioni eccezionalmente elevate e temperature superiori a 1, 000℃.
Il nostro team internazionale ha creato due diversi tipi di diamante a temperatura ambiente e in pochi minuti. È la prima volta che i diamanti vengono prodotti con successo in un laboratorio senza l'aggiunta di calore.
I nostri risultati sono pubblicati sulla rivista Piccolo .
C'è più di una forma di diamante
Gli atomi di carbonio possono legarsi insieme in diversi modi per formare materiali diversi tra cui grafite nera morbida e diamante trasparente duro.
Esistono molte forme ben note di carbonio con un legame simile alla grafite, compreso il grafene, il materiale più sottile mai misurato. Ma sapevi che esiste anche più di un tipo di materiale a base di carbonio con un legame simile al diamante?
In un diamante normale, gli atomi sono disposti in una struttura cristallina cubica. Però, è anche possibile disporre questi atomi di carbonio in modo che abbiano una struttura cristallina esagonale.
Questa diversa forma di diamante si chiama Lonsdaleite, prende il nome dalla cristallografa irlandese e Fellow della Royal Society Kathleen Lonsdale, che ha studiato la struttura del carbonio utilizzando i raggi X.
C'è molto interesse per Lonsdaleite, poiché si prevede che sia il 58% più duro del diamante normale, che è già considerato il materiale più duro presente in natura sulla Terra.
È stato scoperto per la prima volta in natura, nel sito del cratere meteoritico Canyon Diablo in Arizona. Da allora piccole quantità della sostanza sono state sintetizzate nei laboratori riscaldando e comprimendo la grafite, utilizzando una pressa ad alta pressione o esplosivi.
La nostra ricerca mostra che sia la Lonsdaleite che il diamante normale possono essere formati a temperatura ambiente in un ambiente di laboratorio, semplicemente applicando alte pressioni.
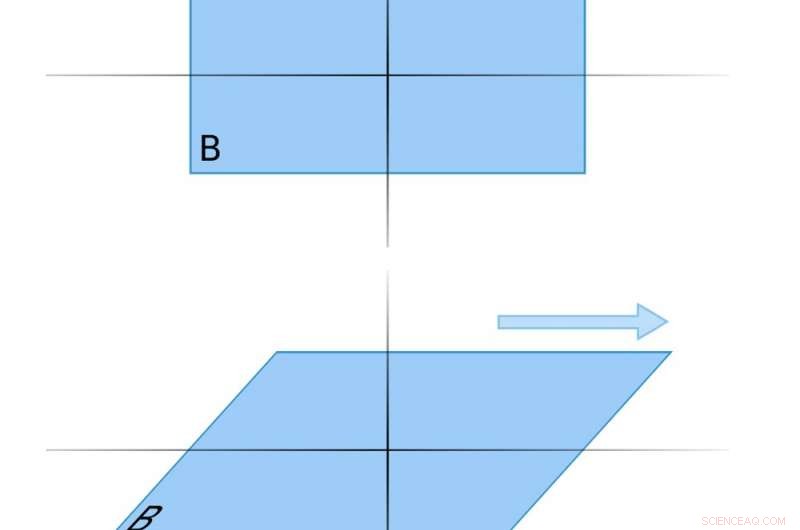
Nelle forze di "taglio", l'oggetto viene spinto in una direzione a un'estremità, e la direzione opposta all'altra. Credito:Wiki Commons
I tanti modi per fare un diamante
I diamanti sono stati sintetizzati nei laboratori fin dal 1954. Poi, Tracy Hall della General Electric li ha creati utilizzando un processo che imitava le condizioni naturali all'interno della crosta terrestre, aggiunta di catalizzatori metallici per accelerare il processo di crescita.
Il risultato è stata l'alta pressione, diamanti ad alta temperatura simili a quelli che si trovano in natura, ma spesso più piccole e meno perfette. Questi sono prodotti ancora oggi, principalmente per applicazioni industriali.
L'altro metodo principale per la produzione di diamanti è tramite un processo chimico-gas che utilizza un piccolo diamante come "seme" per far crescere diamanti più grandi. Sono richieste temperature di circa 800 . Sebbene la crescita sia piuttosto lenta, questi diamanti possono crescere grandi e relativamente privi di difetti.
La natura ha fornito suggerimenti su altri modi per formare il diamante, anche durante il violento impatto di meteoriti sulla Terra, così come in processi come le collisioni di asteroidi ad alta velocità nel nostro sistema solare, creando ciò che chiamiamo "diamanti extraterrestri".
Gli scienziati hanno cercato di capire esattamente come si formano i diamanti da impatto o extraterrestri. Ci sono alcune prove che, oltre alle alte temperature e pressioni, le forze di scorrimento (note anche come forze di "taglio") potrebbero svolgere un ruolo importante nell'innescare la loro formazione.
Un oggetto colpito da forze di taglio viene spinto in una direzione in alto e nella direzione opposta in basso.
Un esempio potrebbe essere spingere un mazzo di carte a sinistra in alto ea destra in basso. Ciò costringerebbe il mazzo a scivolare e le carte ad allargarsi. Quindi, le forze di taglio sono anche chiamate forze "scorrevoli".
Fare diamanti a temperatura ambiente
Per il nostro lavoro, abbiamo progettato un esperimento in cui un piccolo chip di carbonio simile alla grafite è stato sottoposto sia a forze di taglio estreme che a pressioni elevate, favorire la formazione del diamante.

Questa immagine al microscopio elettronico mostra un "fiume" di diamante in un "mare" di lonsdaleite.
A differenza della maggior parte dei lavori precedenti su questo fronte, non è stato applicato alcun riscaldamento aggiuntivo al campione di carbonio durante la compressione. Utilizzando la microscopia elettronica avanzata, una tecnica utilizzata per catturare immagini ad altissima risoluzione, è stato scoperto che il campione risultante conteneva sia diamante normale che Lonsdaleite.
In questa disposizione mai vista prima, un sottile "fiume" di diamante (circa 200 volte più piccolo di un capello umano) era circondato da un "mare" di Lonsdaleite.
La disposizione della struttura ricorda le "fasce di taglio" osservate in altri materiali, in cui un'area ristretta sperimenta intensa, ceppo localizzato. Ciò suggerisce che le forze di taglio siano state la chiave per la formazione di questi diamanti a temperatura ambiente.
Noci dure da rompere
La capacità di produrre diamanti a temperatura ambiente, in pochi minuti, apre numerose possibilità di produzione.
Nello specifico, rendere la Lonsdaleite "più dura del diamante" in questo modo è una notizia entusiasmante per le industrie in cui sono necessari materiali estremamente duri. Per esempio, il diamante viene utilizzato per rivestire punte e lame per prolungare la durata di questi strumenti.
La prossima sfida per noi è abbassare la pressione necessaria per formare i diamanti.
Nella nostra ricerca, la pressione più bassa a temperatura ambiente in cui si sono formati i diamanti era di 80 gigapascal. Questo è l'equivalente di 640 elefanti africani sulla punta di una scarpa da ballo!
Se sia il diamante che la Lonsdaleite potessero essere prodotti a pressioni inferiori, potremmo farne di più, più veloce ed economico.
Questo articolo è stato ripubblicato da The Conversation con una licenza Creative Commons. Leggi l'articolo originale. 