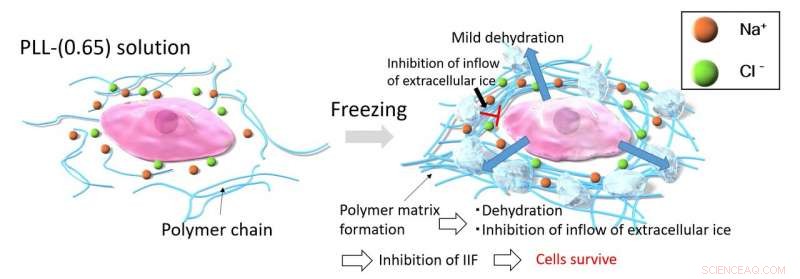
Quando le cellule sono congelate con PLL-(0.65), il processo di congelamento concentra le molecole di PLL-(0.65), che a sua volta li fa aggregare a causa di forti forze attrattive intermolecolari. Questa aggregazione di PLL-(0.65) intrappola ioni e acqua nella matrice per prevenire qualsiasi drammatico cambiamento osmotico. La spessa matrice polimerica inibisce l'afflusso di ghiaccio extracellulare nelle cellule, che evita il problema della formazione di ghiaccio intracellulare (IIF). Immagine per gentile concessione:Kazuaki Matsumura del JAIST.
La crioconservazione comporta la conservazione di materiali biologici, come le cellule, tessuti, e organi, a temperature bassissime in modo che possano essere ravvivati e utilizzati in un secondo momento. Per ottenere una crioconservazione tale che i materiali conservati non vengano danneggiati, gli scienziati usano varie sostanze chimiche chiamate crioprotettori, che facilitano il processo di congelamento. Sfortunatamente, molti degli agenti crioprotettivi esistenti hanno importanti limitazioni. Per esempio, il dimetilsolfossido è utile per la crioconservazione dei globuli rossi, ma è anche tossico per le cellule.
Per superare questi limiti, i ricercatori del Japan Advanced Institute of Science and Technology (JAIST) e del RIKEN giapponese hanno sperimentato una classe di sostanze chimiche note come polianfoliti, identificando un poliamfolita chiamato -poli-ʟ-lisina carbossilata (COOH-PLL) come un promettente crioprotettore che non ha effetti tossici sulle cellule.
Però, il meccanismo con cui COOH-PLL agisce come crioprotettore è rimasto poco compreso, e questo ha ostacolato gli sforzi per sviluppare crioprotettori di poliamfoliti migliori. Per colmare questa lacuna conoscitiva, questo team di ricercatori, che era guidato dal professor Kazuaki Matsumura di JAIST e che includeva anche Asst. Il prof. Robin Rajan di JAIST e il dott. Fumiaki Hayashi e il dott. Toshio Nagashima di RIKEN hanno condotto un altro studio in cui hanno utilizzato un metodo chiamato spettroscopia di risonanza magnetica nucleare (NMR) allo stato solido per caratterizzare ciò che accade alle molecole d'acqua, ioni sodio e cloruro, e una forma di COOH-PLL chiamata PLL-(0.65) quando vengono miscelati e congelati alle temperature utilizzate nella crioconservazione. I loro risultati appaiono in un recente numero della rivista peer-reviewed Communications Materials.
Come previsto, i segnali NMR registrati da queste soluzioni congelate indicavano una ridotta mobilità a livello molecolare e una maggiore viscosità della soluzione (cioè, maggiore resistenza al flusso) a temperature ultra-basse. È importante sottolineare che le molecole PLL-(0.65) intrappolavano le molecole d'acqua e gli ioni in modi che impedivano la formazione di cristalli di ghiaccio intracellulari e contrastavano gli effetti dello shock osmotico (una forma di disfunzione fisiologica in cui un improvviso cambiamento nelle concentrazioni di ioni intorno a una cellula può portare a rapido afflusso o deflusso di fluido nella o dalla cellula, danneggiandolo). I cristalli di ghiaccio intracellulari e lo shock osmotico sono le principali cause di danno cellulare o tissutale durante il congelamento, quindi la capacità di PLL-(0.65) di prevenire entrambi aiuta a spiegare la sua efficacia come crioprotettore.
Nel descrivere il valore scientifico di questi risultati, Il prof. Matsumura osserva che l'uso della NMR "ha permesso la caratterizzazione delle proprietà crioprotettive di polimeri che operano attraverso meccanismi diversi da quelli degli attuali crioprotettori". Egli prevede che questa caratterizzazione "faciliterà la progettazione molecolare di nuovi crioprotettori, " che "promuoverà l'uso clinico di agenti crioprotettivi polimerici che possono fungere da efficienti alternative agli agenti a piccole molecole come il dimetilsolfossido e il glicerolo".
I crioprotettori a piccole molecole sono utili solo per preservare cellule e piccoli tessuti, ma i crioprotettori polimerici possono consentire ai ricercatori di ottenere la crioconservazione di volumi di tessuto più grandi o addirittura di interi organi. Questo sarebbe un importante passo avanti per campi emergenti come la medicina rigenerativa, che mira a ripristinare le normali funzioni fisiologiche sostituendo o rigenerando le cellule, tessuti, e organi.
I risultati del team potrebbero anche avere importanti implicazioni per la biologia di base. Negli ultimi anni, gli scienziati hanno scoperto che le proteine intrinsecamente disordinate, che mancano di una forma tridimensionale fissa, svolgono un ruolo importante nella protezione delle cellule dai danni legati all'essiccazione e allo shock osmotico alle basse temperature. Poiché le proteine sono esse stesse una classe di polianfoliti, questi risultati recentemente pubblicati sul comportamento di COOH-PLL a temperature ultra-basse possono aiutare a spiegare i meccanismi con cui le proteine intrinsecamente disordinate proteggono le cellule. Ulteriori ricerche sui meccanismi di tali proteine possono a loro volta portare allo sviluppo di materiali avanzati con usi nella medicina rigenerativa.
In conclusione, questi risultati possono essere di notevole valore per la biologia e la medicina. "Sulla base della nostra comprensione ora migliorata dei meccanismi degli agenti crioprotettivi polimerici, " nota il prof. Matsumura, "prevediamo di sviluppare nuove tecnologie di crioconservazione per grandi volumi di tessuti e organi, che consentirà l'implementazione su scala industriale della medicina rigenerativa attraverso la creazione di banche di tessuti ingegnerizzati." Questi passi verso la medicina rigenerativa faranno molto per migliorare la vita delle persone che vivono con disturbi medici che sono attualmente incurabili.