Credito:Wiley
Il trasferimento accoppiato di ossigeno e le reazioni di trasferimento di elettroni che utilizzano cofattori sono reazioni enzimatiche di importanza cruciale per tutte le forme di vita, dai batteri ai vertebrati. Nel European Journal of Inorganic Chemistry , gli scienziati hanno introdotto un modello per l'enzima solfito ossidasi. Si basa su un complesso di molibdeno i cui speciali ligandi possono essere ossidati per consentire l'accoppiamento del trasferimento di ossigeno a un substrato con un trasferimento di elettroni intramolecolari. Gli intermedi contenenti molibdeno (V)-ione svolgono un ruolo critico.
Molti enzimi non funzionano da soli; richiedono cofattori, componenti non proteici che svolgono un ruolo nel trasferimento di elettroni. Questi spesso coinvolgono ioni metallici, come il ferro nei citocromi o l'oligoelemento molibdeno, che si trova nelle ossotransferasi di molibdeno, enzimi che trasferiscono gli atomi di ossigeno ai substrati. Un importante rappresentante di quest'ultimo è la solfito ossidasi, che ossida il solfito tossico per produrre solfato. Il trasferimento di ossigeno comporta un cambiamento nello stato di ossidazione del molibdeno da tetravalente (MoIV) a pentavalente (MoV). Gli elettroni coinvolti vengono rimossi tramite citocromi e utilizzati per la produzione di ATP. Il molibdeno pentavalente (MoV) sembra essere un intermedio nella reazione.
I ricercatori che lavorano con Katja Heinze presso l'Università di Mainz hanno ora sviluppato un approccio concettuale per stabilizzare e caratterizzare spettroscopicamente gli intermedi previsti nelle reazioni delle ossotransferasi contenenti Mo utilizzando sistemi modello. Usano un metodo che viene utilizzato anche nel controllo dei catalizzatori:collegano un "interruttore" molecolare con uno stato di ossidazione controllabile.
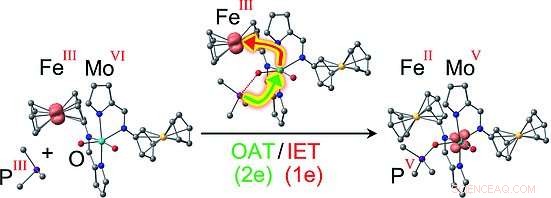
I ricercatori hanno scelto di utilizzare la coppia redox ferrocene/ferrocenio, in cui un atomo di ferro è racchiuso tra due carichi negativamente, aromatico, anelli di carbonio a cinque membri. Lo ione ferro può passare da uno stato con una doppia carica positiva (FeII, ferrocene) e una triplice carica positiva, stato ossidato (FeIII, ferrocenio). Questo è analogo ai cofattori del citocromo presenti in natura, che può contenere anche FeII o FeIII. I ricercatori hanno collegato due di questi "interruttori" ferrocene/ferrocenio a un complesso di molibdeno come modello per il centro attivo di una solfito ossidasi. Il molibdeno è nello stato di ossidazione VI e ha due atomi di ossigeno attaccati da doppi legami. La reazione con un fosfano organico (una molecola di fosforo-idrocarburo) come substrato modello accettore di ossigeno avviene a velocità variabili, a seconda delle cariche sugli "interruttori", perché lo stato redox dei sostituenti ferrocenilici modula le barriere energetiche per alcuni intermedi. Ciò si traduce in una varietà di addotti tra il complesso Mo e il fosfano.
Le versioni più interessanti sono quelle con due ioni FeIII o uno FeII e uno FeIII:in questi casi, il meccanismo non è più un semplice trasferimento di un atomo di ossigeno al substrato, come per la versione FeII/FeII. Invece è accoppiato a un trasferimento di elettroni intramolecolari, possibilmente concettualmente simile a quello delle ossidasi solfito naturali. Durante la reazione di trasferimento dell'ossigeno, un elettrone viene trasferito dal molibdeno a uno degli ioni FeIII, risultante in una distribuzione di carica di FeII FeIII MoV o FeII FeII MoV. Per quest'ultima versione, i ricercatori sono stati in grado di utilizzare la spettroscopia di risonanza di spin elettronico per rilevare in modo inequivocabile l'intermedio MoV FeII FeII MoV con il substrato ossidato (il prodotto) ancora legato ad esso. L'accoppiamento del trasferimento di ossigeno a un trasferimento di elettroni intermolecolari abbassa la barriera di attivazione per questa fase di reazione e contemporaneamente stabilizza l'intermedio MoV, come previsto dai modelli informatici.
I ricercatori propongono di utilizzare questo nuovo sistema come modello per il trasferimento dell'atomo di ossigeno e le fasi di trasferimento intramolecolare di elettroni nelle ossidasi solfito, e sperare di utilizzare questo nuovo concetto per sviluppare analoghi per ulteriori reazioni enzimatiche con trasferimento di elettroni accoppiati. Nel futuro, sembra anche possibile estendere questo concetto a reazioni catalitiche commutabili che non hanno un prototipo naturale.