
Una nuova ricerca del MIT descrive come i microrganismi marini contribuiscono a uno strato di nitrito appena sotto la zona illuminata dal sole dell'oceano. Credito:Massachusetts Institute of Technology
L'azoto è un prodotto caldo nell'oceano di superficie. I produttori primari, tra cui fitoplancton e altri microrganismi, lo consumano e lo trasformano in molecole organiche per costruire biomassa, mentre altri trasformano forme inorganiche per accedere alla loro riserva chimica di energia. Tutti questi passaggi fanno parte del complesso ciclo dell'azoto della colonna d'acqua superiore.
Circa 200 metri più in basso, appena sotto la zona illuminata dal sole dell'oceano, risiede uno strato di nitrito, un composto intermedio nel ciclo dell'azoto. Gli scienziati hanno scoperto questa robusta caratteristica, chiamato il massimo dei nitriti primari, negli oceani ossigenati del mondo. Sebbene siano state avanzate diverse ipotesi individuali, nessuno ha spiegato in modo convincente questa firma marina fino ad ora.
Un recente Comunicazioni sulla natura studio condotto da ricercatori del Programma in Atmosfere, Oceani e clima (PAOC) all'interno del Dipartimento della Terra del MIT, Le scienze atmosferiche e planetarie (EAPS) utilizzano la teoria, modellazione, e dati osservativi per studiare i meccanismi ecologici che producono l'accumulo di nitrito osservato e ne determinano la posizione nella colonna d'acqua. L'autrice principale Emily Zakem, un'ex studentessa laureata EAPS che ora è postdoc presso la University of Southern California, insieme alla ricercatrice scientifica principale EAPS Stephanie Dutkiewicz e al professor Mick Follows mostrano che i vincoli fisiologici e la competizione di risorse tra il fitoplancton e i microrganismi nitrificanti nello strato illuminato dal sole può produrre questo tratto oceanico.
Regolazione della pompa biologica
Nonostante la sua bassa concentrazione oceanica, il nitrito (NO2-) svolge un ruolo chiave nei cicli globali del carbonio e dell'azoto. La maggior parte dell'azoto nell'oceano risiede nella forma inorganica di nitrato (NO3-), quali produttori primari e microrganismi lo riducono chimicamente per costruire molecole organiche. La remineralizzazione si verifica quando avviene il processo inverso:il fitoplancton e altri batteri eterotrofi scompongono questi composti organici in ammonio (NH4+), una forma di azoto inorganico. L'ammonio può quindi essere nuovamente consumato dai produttori primari, che traggono la loro energia dalla luce. Anche altri microrganismi chiamati chemioautotrofi utilizzano l'ammonio sia per produrre nuova biomassa sia come fonte di energia. Per fare questo, estraggono ossigeno dall'acqua di mare e la trasformano, un processo chiamato nitrificazione, che avviene in due fasi. Primo, i microbi convertono l'ammonio in nitrito e poi in nitrato.
Da qualche parte lungo la linea, il nitrito si è accumulato alla base della zona illuminata dal sole, che ha implicazioni per la biogeochimica oceanica. "A grandi linee, stiamo cercando di capire cosa controlla la remineralizzazione della materia organica nell'oceano. È quella remineralizzazione che è responsabile della formazione della pompa biologica, che è lo stoccaggio extra di carbonio nell'oceano a causa dell'attività biologica, " dice Zakem. È questa forte influenza che l'azoto ha sul ciclo globale del carbonio che cattura l'interesse di Follows. "La crescita del fitoplancton sul nitrato è chiamata "nuova produzione" e bilancia la quantità che sta affondando dalla superficie e controlla la quantità di carbonio è immagazzinato nell'oceano. La crescita del fitoplancton sull'ammonio è chiamata produzione riciclata, che non aumenta lo stoccaggio del carbonio oceanico, " Segue dice. "Quindi desideriamo capire cosa controlla i tassi di approvvigionamento e il relativo consumo di queste diverse specie di azoto".
Battaglia per l'azoto
Il massimo di nitrito primario risiede tra due gruppi di microrganismi nella maggior parte degli oceani del mondo. Sopra di esso nella zona illuminata dal sole ci sono il fitoplancton, e nel massimo dei nitriti primari e leggermente al di sotto di questo riposa un'abbondanza di microbi nitrificanti in un'area con alti tassi di nitrificazione. I ricercatori classificano questi microbi in due gruppi in base alla loro fonte di azoto preferita:gli organismi ossidanti dell'ammonio (AOO) e gli organismi ossidanti del nitrito (NOO). Ad alte latitudini come le regioni subpolari della Terra, il nitrito si accumula nella zona illuminata dal sole superficiale e più in profondità.
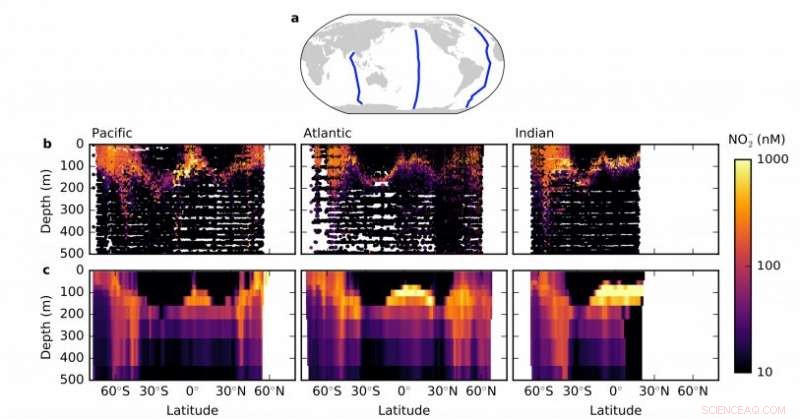
Un modello di ecosistema mostra le concentrazioni di nitrito per profondità (profilo verticale) attraverso tre transetti oceanici. Credito:Massachusetts Institute of Technology
Gli scienziati hanno ipotizzato che potrebbero esserci due ragioni non si escludono a vicenda per l'accumulo di nitrito:nitrificazione da microbi chemioautotrofi, e quando è stressato, il fitoplancton può ridurre i nitrati in nitriti. Poiché l'evidenza isotopica non supporta quest'ultima, il gruppo ha esaminato il primo.
"L'ipotesi di vecchia data era che le posizioni della nitrificazione fossero controllate dall'inibizione della luce di questi microrganismi [nitrificanti], quindi i microrganismi che effettuano questo processo sono stati limitati dalla superficie, "Zakem dice, implicando che questi chemioautotrofi nitrificanti si siano bruciati dal sole. Ma invece di presumere che fosse vero, il gruppo ha esaminato le interazioni ecologiche tra questi e altri organismi nell'oceano di superficie, lasciando che le dinamiche ricadano naturalmente. Per fare questo hanno raccolto campioni microbici dal Pacifico settentrionale subtropicale e li hanno valutati per i tassi di metabolismo, efficienza e abbondanza, e ha valutato i bisogni fisiologici ei vincoli dei diversi microbi nitrificanti riducendo la complessità biologica del loro metabolismo fino alla sua chimica sottostante e ipotizzando così alcuni dei vincoli più fondamentali. Hanno usato queste informazioni per informare le dinamiche dei microbi nitrificanti in un modello biogeochimico sia unidimensionale che tridimensionale.
Il gruppo ha scoperto che, utilizzando questo quadro, potrebbero risolvere le interazioni tra questi chemioautotrofi nitrificanti e il fitoplancton e quindi simulare l'accumulo di nitrito al massimo nitrito primario nelle sedi appropriate. Nell'oceano di superficie quando l'azoto inorganico è un fattore limitante, il fitoplancton e i microbi ossidanti dell'ammonio hanno capacità simili di acquisire ammonio, ma poiché il fitoplancton ha bisogno di meno azoto per crescere e avere un tasso di crescita più rapido, sono in grado di competere con i nitrificatori, escludendoli dalla zona illuminata dal sole. In questo modo, sono stati in grado di fornire una spiegazione ecologica per dove avviene la nitrificazione senza dover fare affidamento sull'inibizione della luce che detta il luogo.
Il confronto delle fisiologie fondamentali dei nitrificanti ha rivelato che le differenze nel metabolismo e nella dimensione delle cellule potrebbero spiegare l'accumulo di nitriti. I ricercatori hanno scoperto che la seconda fase del processo di nitrificazione eseguita dagli ossidanti del nitrito richiede più azoto per la stessa quantità di biomassa creata da questi organismi, il che significa che gli ossidanti dell'ammoniaca possono fare di più con meno, e che ci sono meno ossidanti di nitrito rispetto agli ossidanti di ammoniaca. I microbi ossidanti nitrito hanno anche un vincolo superficie-volume maggiore rispetto ai microbi ossidanti ammonio più piccoli e onnipresenti, rendendo più difficile l'assorbimento dell'azoto. "Questa è una spiegazione alternativa del perché i nitriti dovrebbero accumularsi, " Zakem dice. "Abbiamo due ragioni che puntano nella stessa direzione. Non riusciamo a distinguere quale sia, ma tutte le osservazioni sono coerenti con uno di questi due o con una combinazione di entrambi che è il controllo."
I ricercatori sono stati anche in grado di utilizzare un modello climatico globale per riprodurre un accumulo di nitrito nella zona illuminata dal sole di luoghi come le regioni subpolari, dove il fitoplancton è limitato da un'altra risorsa diversa dall'azoto come la luce o il ferro. Qui, i nitrificanti possono coesistere con il fitoplancton poiché hanno più azoto a loro disposizione. Inoltre, lo strato misto profondo nell'acqua può sottrarre risorse al fitoplancton, dando ai nitrificatori una migliore possibilità di sopravvivenza in superficie.
"C'è questa ipotesi di vecchia data che i nitrificatori siano stati inibiti dalla luce ed è per questo che esistono solo nel sottosuolo, " Dice Zakem. "Stiamo dicendo che forse abbiamo una spiegazione più fondamentale:che questa leggera inibizione esiste perché l'abbiamo osservata, ma questa è una conseguenza dell'esclusione a lungo termine dalla superficie".
Pensare in grande
"Questo studio ha riunito la teoria, simulazioni numeriche, e osservazioni per separare e fornire una semplice descrizione quantitativa e meccanicistica di alcuni fenomeni che erano misteriosi nell'oceano, " Segue dice. "Questo ci aiuta a mettere in discussione il ciclo dell'azoto, che ha un impatto sul ciclo del carbonio. Ha anche aperto la strada all'utilizzo di questo tipo di strumenti per affrontare altre questioni nell'oceanografia microbica." Osserva che il fatto che questi microbi stiano trasformando l'ammonio in nitrato vicino alla zona illuminata dal sole complica la storia dello stoccaggio del carbonio nell'oceano.
Due ricercatori non coinvolti nello studio, Karen Casciotti, professore associato presso il Dipartimento di Scienze del Sistema Terra della Stanford University, e Angela Landolfi, uno scienziato nel dipartimento di modellazione biogeochimica marina presso il GEOMAR Helmholtz Center for Ocean Research Kiel, essere d'accordo. "Questo studio è di grande importanza in quanto fornisce prove di come i tratti individuali degli organismi influenzano le interazioni competitive tra le popolazioni microbiche e forniscono un controllo diretto sulla distribuzione dei nutrienti nell'oceano, " dice Landolfi. "In sostanza Zakem et al., fornire una migliore comprensione del legame tra i diversi livelli di complessità dall'individuo alla comunità fino al livello ambientale, fornendo un quadro meccanicistico per prevedere i cambiamenti nella composizione della comunità e il loro impatto biogeochimico sotto i cambiamenti climatici, "dice Landolfi.
Questa storia è stata ripubblicata per gentile concessione di MIT News (web.mit.edu/newsoffice/), un popolare sito che copre notizie sulla ricerca del MIT, innovazione e didattica.