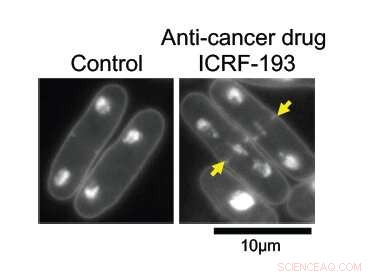
Con DNA topoisomerasi II (topo II) intatto, Il DNA nelle cellule di lievito di fissione si replica normalmente ed è diviso equamente tra due cellule figlie (a sinistra). Quando si è sotto gli effetti del farmaco antitumorale ICRF-193, il DNA si aggroviglia al centro della cellula madre, impedendo la sua netta divisione. Credito:Okinawa Institute of Science and Technology Graduate University
Proprio come i lacci delle scarpe o le collane pendenti, I filamenti di DNA possono aggrovigliarsi in nodi ribelli. Enzimi specializzati mantengono il DNA organizzato quando le cellule si dividono, quindi le cellule si dividono senza problemi e non si bloccano. Ma nelle cellule tumorali, questo failsafe consente al cancro di diffondersi. Ora, scienziati dell'Okinawa Institute of Science and Technology Graduate University (OIST) hanno scoperto come funziona questo meccanismo nel lievito di fissione e come potrebbe essere compromesso nel cancro umano.
Lo studio, pubblicato online l'11 gennaio 2019 di Journal of Biological Chemistry , si concentra su un obiettivo ben consolidato della terapia del cancro:DNA topoisomerasi II, o topo II in breve. Topo II regola la topologia del DNA, gestire la struttura mutevole dei filamenti nel tempo. Le cellule cancerose mostrano una maggiore attività topo II, che a sua volta stimola la crescita del tumore. I farmaci antitumorali Topo II sopprimono la funzione dell'enzima, impedire alle cellule tumorali di replicarsi e ostacolare la diffusione del cancro.
Ma i farmaci topo II esistenti hanno mostrato un successo limitato:gli scienziati hanno bisogno di saperne di più sul meccanismo di base prima di poterlo smussare efficacemente.
"Molti ricercatori stanno lavorando su topo II, ma utilizzano principalmente cellule eucariotiche umane o superiori, " ha detto il dottor Norihiko Nakazawa, primo autore dello studio e scienziato dello staff dell'OIST G0 Cell Unit, guidato dal Prof. Mitsuhiro Yanagida. L'Unità ha scelto di studiare la topo II nel lievito di fissione perché i suoi meccanismi di divisione cellulare sono ampiamente conservati nell'uomo, Egli ha detto, oltre ad essere veloce e facile da manipolare.
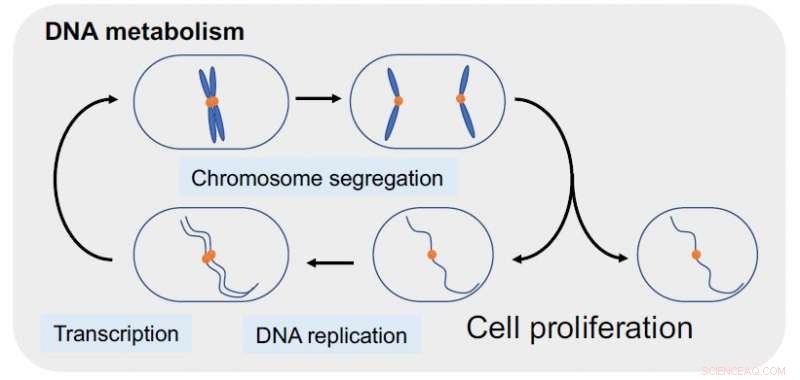
DNA topoisomerasi II (topo II), un regolatore principale del metabolismo del DNA per la proliferazione cellulare, è un obiettivo critico per la terapia antitumorale. Credito:Okinawa Institute of Science and Technology Graduate University
"Possiamo catturare rapidamente la reazione topo II nel lievito, poi passa a studiarlo nelle cellule umane, " ha detto Nakazawa. "Il nostro lavoro mostra che il lievito è un buon modello per lo screening dei farmaci topo II e sarebbe un metodo rapido da utilizzare nelle applicazioni cliniche".
Aumentare l'efficacia dei farmaci antitumorali
I ricercatori miravano a scoprire come opera topo II a livello molecolare. A ingrandimenti maggiori, i suoi effetti sono evidenti; le cellule con l'enzima intatto si dividono normalmente, con metà del loro materiale genetico replicato su ciascun lato della scissione. Senza topo II, il DNA rimane aggrovigliato al centro della cellula madre, impedendo la sua corretta divisione in due cellule figlie.
Ricerche precedenti suggeriscono che la topo II si basa sulla fosforilazione, l'aggiunta di un gruppo fosfato in punti precisi della sua struttura. Nel lievito di fissione e nelle cellule umane, l'enzima caseina chinasi II, noto anche come CKII, interviene per fosforilare regioni specifiche della topo II. In questo lavoro, Nakazawa ha identificato queste regioni e ha scoperto che alcune sono rimaste fosforilate durante l'intero ciclo cellulare. Questo costante scambio chimico ha potenziato l'attività in una regione della topo II nota come "dominio ATPasi". Sebbene i ricercatori abbiano osservato il miglioramento, All'inizio, non potevano dire come effettivamente alterasse la funzione topo II.
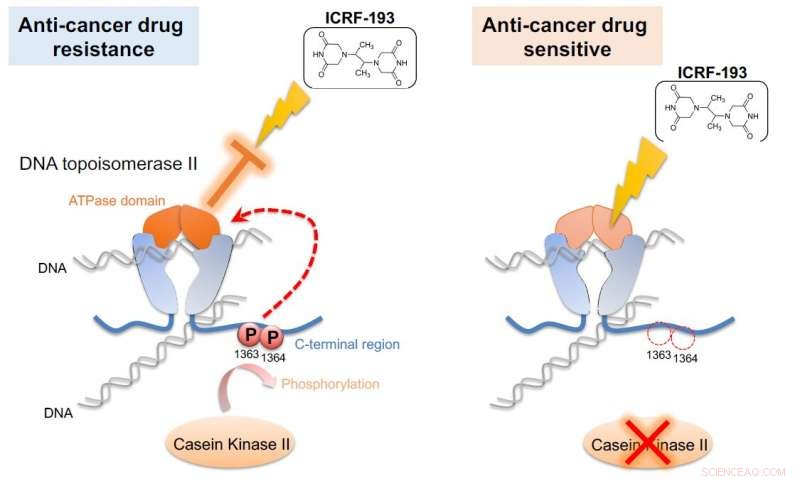
La caseina chinasi II (CKII) fosforila la DNA topoisomerasi II (topo II), attivando così il dominio ATPasi dell'enzima (a sinistra). Questa attivazione annulla gli effetti del farmaco antitumorale ICRF-193. Se l'attività del CKII è attenuata (a destra), l'efficacia di ICRF-193 è salvata. L'unità cellulare G0 ha dimostrato questo meccanismo nel lievito di fissione, un modello semplice che potrebbe essere utilizzato per lo screening dei farmaci antitumorali. Credito:Okinawa Institute of Science and Technology Graduate University
Gli scienziati hanno risolto il puzzle inserendo un farmaco topo II nel mix. Il farmaco ICRF-193 agisce inibendo l'attività dell'ATPasi del topo II, che intrappola efficacemente il DNA in una configurazione stretta in modo che non possa eseguire reazioni enzimatiche. Ma in presenza di CKII, che aumenta l'attività dell'ATPasi, il farmaco è reso inefficace.
"Questo miglioramento [del dominio ATPasi] ha rotto l'effetto del farmaco antitumorale, " disse Nakazawa. "Se blocchiamo la fosforilazione, questa attivazione non avviene e il farmaco rimane efficace".
Potenziale base per nuove terapie
L'evidenza suggerisce che topo II e CKII interagiscono nelle cellule umane proprio come nel lievito di fissione. Le cellule cancerose esprimono livelli più elevati sia di topo II che di CKII rispetto ai tessuti normali, ed entrambi gli enzimi sono stati associati a una proliferazione cellulare anormale. Ora che gli scienziati comprendono il meccanismo alla base del lievito, possono applicare tale conoscenza in studi futuri sulle cellule tumorali umane. un giorno, la ricerca può portare a nuovi trattamenti contro il cancro.
"Se inibiamo CKII e topo II, potrebbe essere un modo molto efficace per inibire la divisione delle cellule cancerose, " ha detto Nakazawa. "Questo effetto additivo potrebbe essere molto potente nella terapia del cancro".