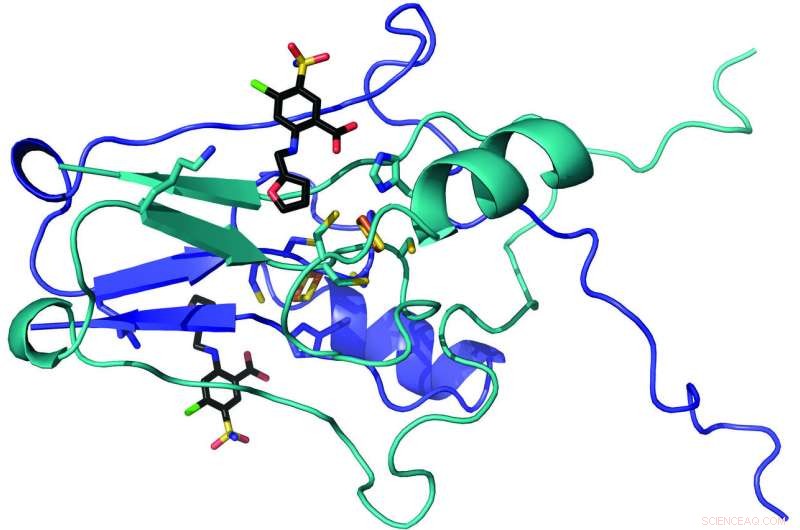
Un team di ricercatori della WVU, tra cui Werner Geldenhuys, John Hollander e Aaron Robart hanno mappato la struttura cristallina di una proteina chiamata "mitoNEET" e hanno individuato il modo in cui un farmaco si attacca ad essa. Poiché la ricerca precedente ha implicato mitoNEET in un diabete, ictus e malattie cardiache, i risultati dei ricercatori possono informare lo sviluppo di nuovi trattamenti per quelle condizioni difficili da affrontare. Credito:West Virginia University
I farmaci si attaccano alle proteine del nostro corpo nello stesso modo in cui i veicoli spaziali attraccano alla Stazione Spaziale Internazionale. Descrivere questo processo in dettaglio può rivelare molto su come funzionano i farmaci e quale forma dovrebbero assumere i nuovi farmaci.
I ricercatori della West Virginia University hanno mappato la struttura cristallina di una proteina che risiede nelle nostre cellule e hanno determinato, per la prima volta, come un farmaco si attacca ad essa. I risultati appaiono in Chimica delle comunicazioni , una rivista di ricerca sulla natura.
Lo studio, finanziato dal West Virginia Clinical and Translational Science Institute, si è concentrato su una proteina chiamata "mitoNEET". MitoNEET abita la membrana esterna dei nostri mitocondri, che agiscono come centrali elettriche che danno energia alle nostre cellule.
"MitoNEET è un nuovo bersaglio terapeutico per le malattie metaboliche e potrebbe portare a trattamenti modificanti la malattia per il morbo di Alzheimer e l'ictus, " disse Werner Geldenhuys, professore associato presso la Scuola di Farmacia e la Scuola di Medicina. Lui e i suoi colleghi, tra cui Aaron Robart, un assistente professore presso la WVU School of Medicine, John Hollander, assistente decano per i programmi professionali della WVU School of Medicine, e Timothy Long, un professore associato della Marshall University School of Pharmacy, ha portato avanti il progetto.
"Questa proteina è stata implicata in molte malattie molto difficili da affrontare:cose come il diabete, ictus, cardiopatia, " ha detto Robart. "In realtà non sappiamo ancora cosa fa la proteina, ma si blocca in prossimità della centrale elettrica della cella, e tutte queste malattie hanno un tema sul flusso di energia".
Per esplorare il ruolo che mitoNEET svolge nei nostri processi energetici, i ricercatori hanno isolato mitoNEET sia dalla sovraespressione batterica che da modelli animali. Quindi hanno sintetizzato 11 molecole simili alla furosemide, un comune diuretico venduto con il marchio LASIX, e hanno esposto loro il mitoNEET.
Dopo che le molecole si sono legate al mitoNEET, i ricercatori hanno costruito mappe atomo per atomo degli accoppiamenti. Hanno controllato a distanza l'Advanced Photon Source dell'Argonne National Laboratory, che bombarda i campioni con raggi X ad alta energia, per rivelare con precisione come le molecole si sono unite.
Il team ha scoperto che le molecole si agganciavano a un gruppo di atomi di ferro e zolfo che facevano parte della proteina. Raisa Nunez, uno studente universitario che partecipa al programma di apprendistato di ricerca, raccolti dati strutturali preliminari. "Ciò evidenzia che una scoperta scientifica significativa può arrivare a qualsiasi livello di carriera, " ha detto Robart.
"Questi risultati sono importanti in quanto ci consentono di continuare a comprendere il ruolo svolto dai mitocondri e dalla bioenergetica in molti stati patologici, "Ha detto Hollander. "La modulazione della funzione mitocondriale attraverso terapie mirate può essere una strada fondamentale per la scoperta di farmaci".
Comprendere la funzione cellulare di mitoNEET potrebbe migliorare le prestazioni dei farmaci che agiscono alterando l'attività della proteina. Per esempio, l'aggiunta di un gruppo di ossigeno in più alla struttura molecolare di un farmaco potrebbe stringere drasticamente il suo legame con mitoNEET ed eliminare il legame involontario con altre proteine cellulari.
Il potenziale risultato per i pazienti che assumono il farmaco? Migliore sollievo dai sintomi.
"Il successo di questo progetto illustra davvero come gli approcci considerati scienza di base possano fornire una visione considerevole dei problemi clinici, " ha detto Michael Schaller, che presiede il Dipartimento di Biochimica della Scuola di Medicina. "Dimostra anche il potere di affrontare i problemi come team composti da membri con competenze molto diverse".